クリニックからのお知らせ
2022.07.13
高血圧治療の新たな展開~ARNIに対する期待~ 森本聡先生
2022年6月27日
演題「高血圧治療の新たな展開~ARNIに対する期待~」
演者: 東京女子医科大学高血圧・内分泌内科准教授 森本 聡 先生
場所: ハイアットリージェンシー横浜
内容及び補足「
血圧を規定する因子
血圧=心拍出量×全末梢血管抵抗(TPVR)=一回拍出量×心拍数×TPVR
一回拍出量:体液量により影響を受ける
一回拍出量および心拍数:心機能により影響を受ける
TPVR:血管症の面積、動脈壁の弾性、血液の粘性により影響を受ける
これらは、腎機能、自律神経系、レニンアルドステロン(RAAS)系によりそれぞれ影響を受ける。
高血圧が持続することにより種々の臓器合併症を起こす。
脳(脳出血、脳梗塞、一過性脳虚血発作等)、心(狭心症、心筋梗塞、心肥大、心不全など)、腎(腎硬化症、腎不全等)、大動脈(大動脈瘤など)、その他の臓器に分けられる。
2017年の我が国の高血圧有病者の治療の有無・コントロール状況の推計を見てみると、コントロール良好の治療者は1/4程度であり、治療中でもコントロール不良者が3割、病期を認識していながら治療を受けていないものが1割:450万人、高血圧の認識がなく治療を受けていない人は1/3:1400万人も存在する。
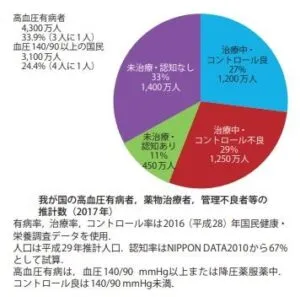
血圧を下げる薬が数多くあり、治療が受けられる環境にありながら、多くの高血圧患者が治療を受けていない『高血圧パラドックス』が大きな問題である。
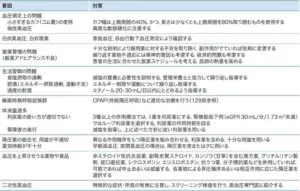
コントロール不良の原因はいくつかある。
血圧測定上の問題:小さすぎるカフとゴム嚢の使用、偽性高血圧
白衣高血圧、白衣現症
アドヒアランス不良
生活習慣の問題(肥満の進行、過度の飲酒)
睡眠時無呼吸症候群
体液過多(食塩摂取の過剰、利尿薬の不適切な使用、腎障害の進行)
降圧薬と拮抗する・あるいはそれ自体で血圧を上昇させる薬物の併用や補助食品の使用
作用機序の類似した降圧薬を併用
二次性高血圧
降圧治療に求められることとしては以下のものがある
- 十分な降圧を得ること
アドヒアランスを上げる
治療効果の実感
投与薬剤数・回数を減らす
- 体液下葉様態を回避
減塩を実行
Na排泄を増やす
- 降圧を超えた臓器保護
RAAS抑制
自律神経活動抑制
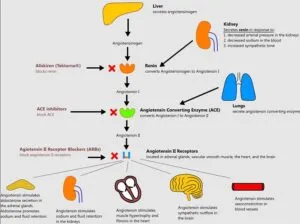
レニン―アンジオテンシン―アルドステロン系(RAAS系)はアンジオテンシン2とアルドステロンを主様な生理活性物質とする系路である。肝臓で合成されたアンジオテンシノーゲンがレニンやACEによってアンジオテンシノーゲン2が生成され、AT1、AT2受容体を介して各臓器に作用する。
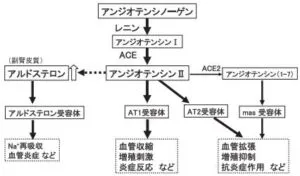
AT1受容体刺激は、血管収縮、Na貯留、心肥大・線維化、動脈硬化を進行させる一方、AT2受容体刺激は、血管拡張、心肥大抑制、線維化抑制、抗動脈硬化作用があると言われている。
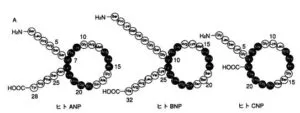
Na利尿ペプチド:ANP、BNP、CNPの三種類のペプチドファミリーで構成されている。
参:ナトリウム利尿ペプチド系には二種類の細胞内情報伝達に与る受容体と一つのクリアランスにかかわる受容体の計3つの受容体がクローニングされている。
GC-AはANP、BNPの受容体であり、GC-BはCNPの受容体である。
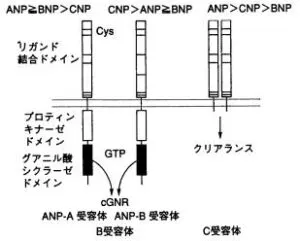
循環器科 Vol.46:p77,1999
ANPは輸入細動脈を拡張させ、輸出細動脈を収縮させて、糸球体内圧上昇、ろ過係数の増加により利尿に働く。集合管においては、管腔側Na+チャンネル阻害、血管側Na+-K+-ATPase阻害によりナトリウム利尿をもたらす。また血管拡張・降圧作用も示す。また、レニン分泌・アルドステロン産生を抑制し、交感神経抑制作用もある。
BNPは豚脳より単離同定され、その後心室内で産生されていることが明らかとなった。
CNPは主に血管内皮細胞で産生されており、血管における局所因子として注目されている。

Am J Physiol Renal Physiol 2015; 308: F1047-1055
BNPの生成・分泌・代謝
心筋内においてproBNPが作成され、furinなどの酵素によって、BNPとNT-proBNPに切断され等モル濃度で血中に放出される。BNPはneutral endopeptidaseによる分解を受けたり、Clearance receptorによるendocytosisを受ける。それ以外のものが腎臓から排泄されるが、NT-proBNPは生体内で群解されないためBNP産生の状態をより正確に反映しているといえる。BNPの血中半減期は20分でNT-proBNPは120分と異なる。
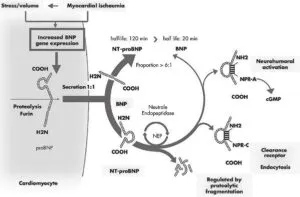
Heart 2006;92:843-849
ネプライシン開発の経緯
心不全治療薬としてANP製剤カルペリチド(ハンプ)があったが注射剤であり、これの内服薬を作りたいというのが切っ掛けだった。ANPの分解酵素『ネプリライシン』の阻害薬を作成しようということになった。
ネプリライシン阻害薬単独ではANP血中濃度の上昇は認めたが、降圧効果が認められなかった。
次にACEIとネプリライシン阻害薬の合剤が作成された。心不全リスクの低下はエナラプリルと同程度で、血管浮腫の発現リスクがエナラプリルの3倍となった。ACE阻害薬とネプリライシン阻害薬がともにブラジキン増加作用を持っていたためとわかり、ARBとの合剤に変更となった。
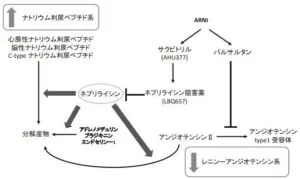
Endocr Connect 2015;4:R25-36
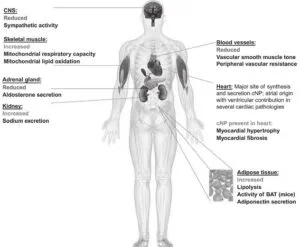
ネプリライシンは5-40アミノ酸残基ほどの長さを有するペプチドを基質としてペプチド内部の疎水アミノ酸残基の前で切断を行う膜結合型のメタロペプチダーゼである。エンンケファリン、ニューロペプチドγ、ソマトスタチン、BNP、ブラジキニン、サブスタンスP、アドレノメデュリン、エンドセリンなどを分解する。また、アルツハイマー病発症の中核的役割を果たすと言われているアミロイドβペプチドの分解に関与する脳内主要酵素である。
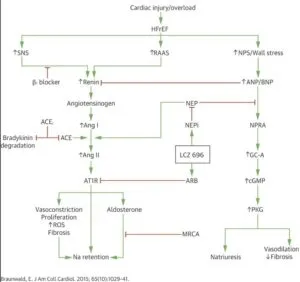
JACC 2015 65, Issue 10, 17 March 2015, Pages 1029-1041
日本人20歳以上の軽度から中等度の高血圧患者1161例に対してARNI 200㎎(387例)とARNI400㎎(385例)、オルメサルタン20㎎(389例)の1日一回8週間投与の比較試験では、オルメサルタンよりも治療効果はよくすぐれた血圧減少をもたらした。
経時変化でも一週間で平均収縮期血圧の低下を認めており、早くて強い降圧効果を実感でき、アドヒアランスの向上が期待できる薬剤である。
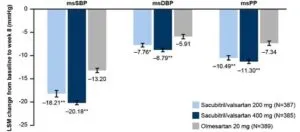
Hypertens Res. 2022 May;45(5):824-833.
https://www.nature.com/articles/s41440-021-00819-7
エンレスト錠市販後調査2021年9月~2022年3月
https://www.okinawa-congre.co.jp/jsh43/files/entresto_flyer.pdf
エンレストはネプリライシン阻害により血管拡張作用、利尿作用、RAAS系抑制作用、交感神経抑制作用、心肥大抑制作用、抗線維化作用、及びアルドステロン分泌抑制作用を有するナトリウム利尿ペプチドの作用亢進に寄与し、AT1受容体拮抗作用により、血管収縮、腎ナトリウム・体液貯留、心肥大、及び心血管リモデリング以上に対する抑制作用をもたらすと考えられる。
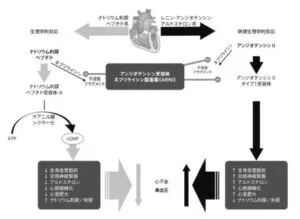
https://www.drs-net.novartis.co.jp/siteassets/common/pdf/enr/if/if_enr_202110.pdf
アンジオテンシン2を介して誘発されたラット心筋細胞の肥大に対する検討ではSacubitrilatとバルサルタン併用で有意に心筋肥大抑制作用は増強された。
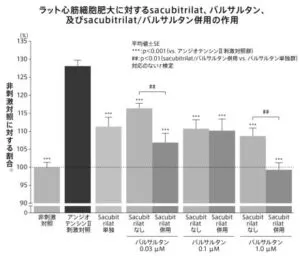
Circ Heart Fail. 2013; 6(3): 594-605
https://www.ahajournals.org/doi/10.1161/CIRCHEARTFAILURE.112.000289
EF≦40%のNYHA2-4の心不全患者8442例をLCZ696投与4187例とエラナプリル投与4212例に分け検討した。Primary endopointはLCZ696群で914例(21.8%)に対し、エナラプリル群では1117例(26.5%)、HR 0.80、全死亡ではLCZ696群で711例(17.0%)、エナラプリル群で835例(19.8%)、HR 0.84と有効性が示された。
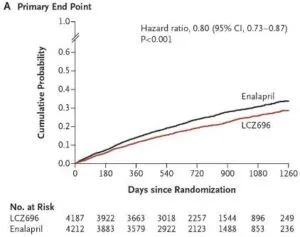
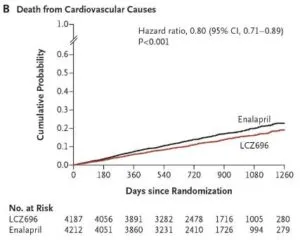
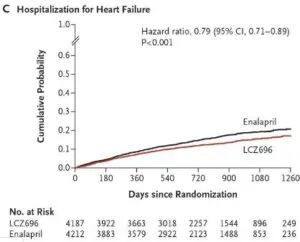
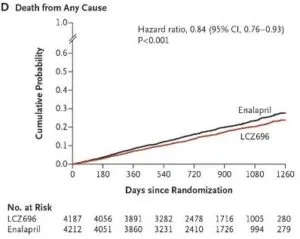
NEJM 2014 371 993-1004
https://www.nejm.org/doi/10.1056/NEJMoa1409077
114例の高血圧患者にARNIとオルメサルタン投与群に二分し12週後、52週後の血圧、左室重量を比較した。降圧効果は52週後の収縮期血圧の他は有意な差を認めなかったが、左室重量はARNI投与群でより低値であった。
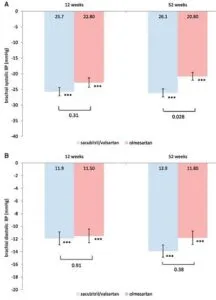
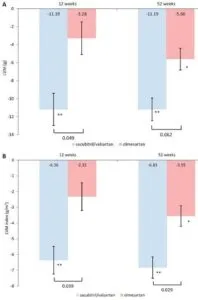
Eur Hear J 2017 38 3300-3317
https://academic.oup.com/eurheartj/article/38/44/3308/4259266
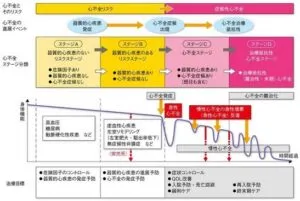
心不全の進行ステージを見てみると、高血圧がすでに心不全においてステージAであり、ARNIはこの時点から投与可能な薬であり、左室肥大の進行を抑制し、心不全の増悪を抑制することが期待できる薬剤である。
腎に及ぼすナトリウムペプチドの生理作用は輸入細動脈の拡張、輸出細動脈の収縮、メサンギウム細胞の弛緩、Kf値を上げる作用、レニン分泌抑制、近位尿細管・集合管のNa再吸収抑制などの効果が考えられている。
日本人の高血圧症及び腎機能障害患者に対してLCZ696の8週間投与において、腎機能の悪化はなく収縮期血圧、拡張期血圧は平均して20.5±11.3mmHg、8.3±6.3mmHg低下した。
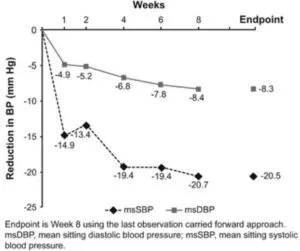
Hypertension Research volume 38, pages269–275 (2015)
https://www.nature.com/articles/hr20151
抹消循環RAAS系:高Na+(Cl-ろ過量の上昇)→レニンの分泌↓→アンギオテンシン2↓+AT1受容体刺激↓→アルドステロン↓→MR刺激↓→腎Na再吸収↓→高Na+に対して抑制的に働く
中枢RAAS系:高Na+(決勝浸透圧の上昇)→血漿バゾプレッシン↑→レニンの分泌↑→アンギオテンシン2↑+AT1受容体刺激↑→アルドステロン↑→MR刺激↑→腎Na再吸収↑→血圧上昇→高Na+に対して促進的に働く
参:塩味感覚はNa+の恒常性にかかわる。体内のNa+濃度は体液浸透圧の保持、神経興奮などの生命維持に不可欠な働きを担うので、常に一定に保たれる必要がある。
体液中のNa+が減少すると、糸球体傍細胞からレニンが放出され、アンジオテンシン2(Ang2)が生成、アルドステロンの放出を促して、腎集合管において上皮性Na+チャンネル(ENaC)を介してNa+の再吸収を促進する。さらに減少すると、生物は“塩味”を手掛かりとして外部からNa+を摂取して体内Na+バランスを維持する。この食塩飢餓状態のときには、通常嫌う高濃度の食塩水、Na+を得意的にこの生んで飲むようになる。この背景に塩味感受性の特異的な低下が起こると考えられている。
塩味受容機構は少なくとも二つの成分:利尿剤アミロライドにより抑制されるAmiloride sensitive(AS)成分と抑制されないAmiloride insensitive(AI)成分に分けられる。
AS成分はNa+に特異的に応答する成分であり、AI成分はNa+以外にもK+やNH4+といった電解質に広く応答する成分である。
近年AS成分はアミロライド感受性上皮型Na+チャンネル(ENaC)αサブユニットであることが明らかになった。
Ang2は、Type1受容体(AT1)を介して、副腎のみならず、血管、脳下垂体、交感神経系など様々な臓器に直接作用し、また脳室内や血液に投与すると、塩分特にNa+嗜好性を高めることや、その効果は投与一時間以内にみられることが報告された。
Ang2は味蕾細胞に発現しているAT1を介して、短時間でENaCを介する塩味感受性を抑制することでNa+摂取量を増やし、引き続き誘導されるアルドステロンは、Na+の体内への吸収を促進するとともに、塩味感受性を上昇させて塩分の摂取をストップさせると考えられる。
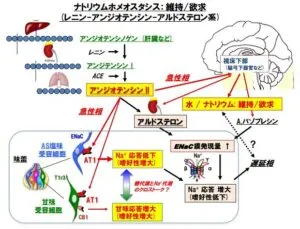
https://www.kyushu-u.ac.jp/f/1186/2013_04_09.pdf
Journal of Neuroscience 10 April 2013, 33 (15) 6267-6277
https://www.jneurosci.org/content/33/15/6267