川村所長の勉強会参加記録
2014.08.11
心疾患治療におけるRAASの重要性 瀬在明 先生
2014年7月28日 横浜ベイホテル東急
演題「心疾患治療におけるRAASの重要性 ~心保護、腎保護をいかに行うか~」
演者:日本大学医学部外科学系 心臓血管・呼吸器・総合外科学分野講師 瀬在明 先生
内容及び補足「
手術時においては、神経系の刺激のみならず様々なホルモンが分泌されており、各種臓器への血流変化が生じ、代謝変化も生じている。
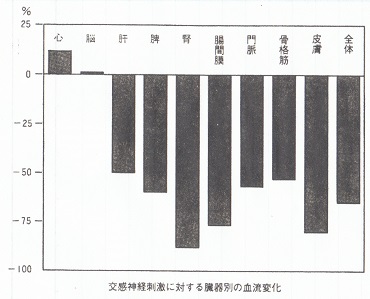
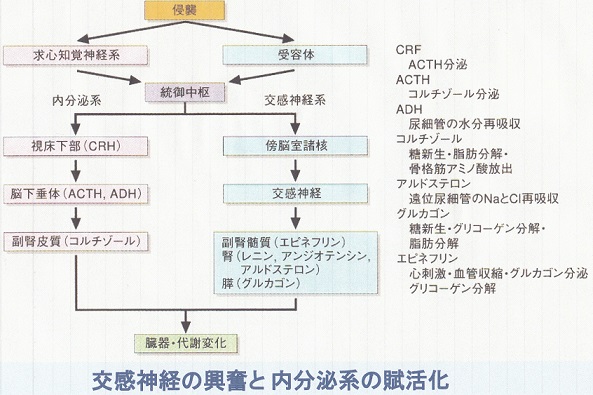
これらの結果生体機能の変化が生じ、その上に、麻酔薬の効果が上乗せされる。
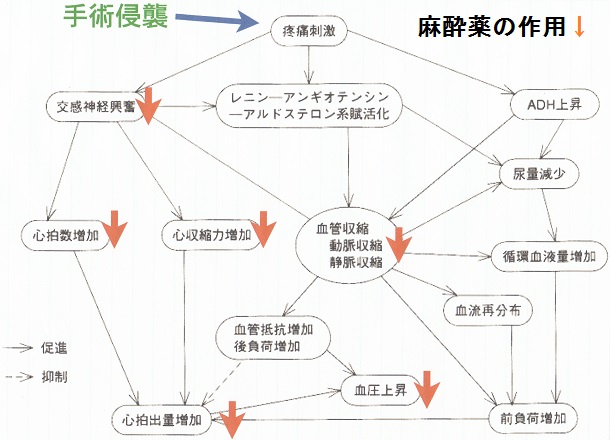
1216例の急性冠不全症候群症例に対して緊急PCI療法を行った直後からカルペリチド(hANP)を追加投与した群とそうでない群の比較試験J-WIND試験が行われ、急性期の心筋梗塞サイズの縮小と、慢性期の有意な心機能改善を認めた。
http://www.thelancet.com/journals/lancet/article/PIIS0140-6736(07)61634-1/fulltext
心臓の手術中から少量のhANPを持続的に投与することにより、血中のレニンやアンジオテンシンⅡの濃度を抑制し、GFR量を維持し、尿量を確保するので、術後に投与する利尿剤の必要量が減少し胸水量も減少することが示された。
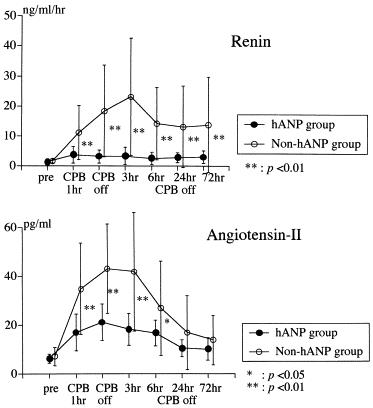
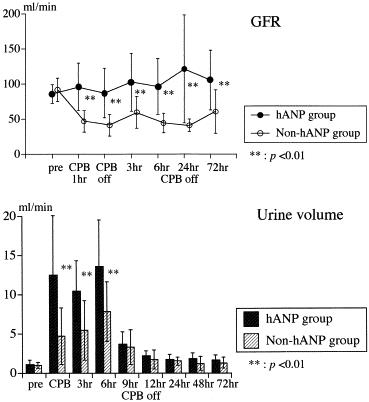
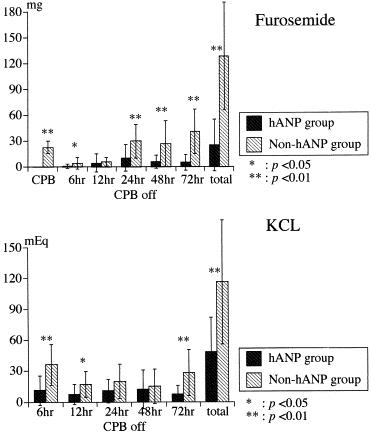
人工心肺装置cardiopulmonary bypass (CPB)を回す心臓手術の際にレニン・アンジオテンシン・アルドステロン系を抑制するhANPの少量持続投与により、早期や長期の死亡率には差が出なかったが、5から8年の心臓死はhANOP投与群で1.5%に対し、コントロール群では14.5%と有意な差を認めた。

(A) The overall survival rate showed no significant difference between the 2 groups. (B) The cardiac death-free rate was significantly higher in the human atrial natriuretic peptide (hANP) group than in the placebo group. (C) The cardiac event-free rate was significantly higher in the hANP group than in the placebo group. Solid lines = hANP group; dashed lines = placebo group.
http://www.annalsthoracicsurgery.org/article/S0003-4975(99)01305-3/fulltext
冠動脈バイパス術を行った症例においてhANPを投与するとクレアチニンクリアランスの悪化を予防できた。
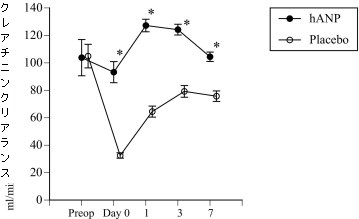
Creatinine clearance was significantly higher in the human atrial natriuretic peptide (hANP) group from post-operative day 0 to week 1. *p < 0.05.
hANPの投与により、血中のレニンの分泌が抑制され、アンジオテンシンⅡの濃度及びアルドステロンの濃度も抑制された。
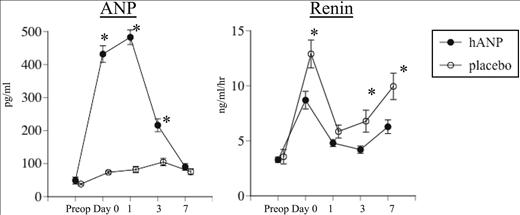
Atrial natriuretic peptide (ANP) increased rapidly in the human atrial natriuretic peptide (hANP) group and was significantly higher than in the placebo group until post-operative day 3, but there was no significant difference between the 2 groups at post-operative week 1. Renin was significantly lower in the hANP group excluding day 1. *p < 0.05.
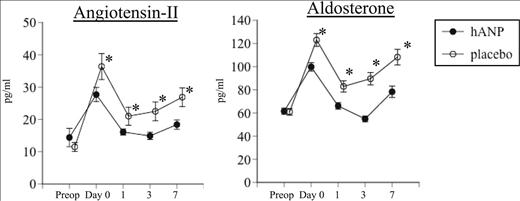
The levels of angiotensin-II and aldosterone increased post-operatively in the placebo group, and reached a peak at the time of the return to intensive care unit. Angiotensin-II and aldosterone were significantly lower in the human atrial natriuretic peptide (hANP) group throughout the study. *p < 0.05.
http://content.onlinejacc.org/article.aspx?articleID=1140048
慢性腎臓疾患CKDがある患者さんにおいてCABG手術を施行した際にhANPの投与は、死亡率には影響しなかったが、術後早期に透析に至る症例が減少し、血清クレアチニン値の上昇を抑制できた。
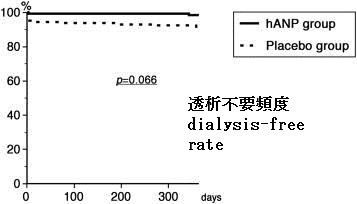
The dialysis-free rate was significantly higher in the human atrial natriuretic peptide (hANP) group (solid line) than in the placebo group (dashed line).
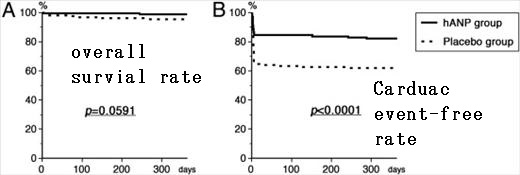
(A) The overall survival rate showed no significant difference between the 2 groups.
(B) The cardiac event-free rate was significantly higher in the human atrial natriuretic peptide (hANP) group (solid lines) than in the placebo group (dashed lines).
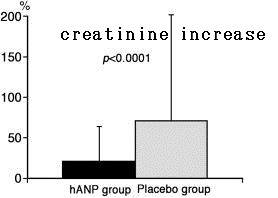
Creatinine increase was 21.6 ± 42.8% in the human atrial natriuretic peptide (hANP) group and 71.1 ± 130.6% in the placebo group, being significantly higher in the placebo group.
http://content.onlinejacc.org/article.aspx?articleID=1206903
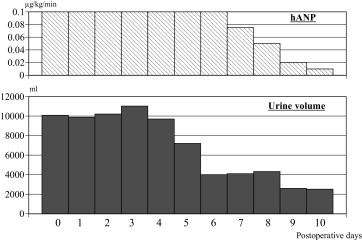
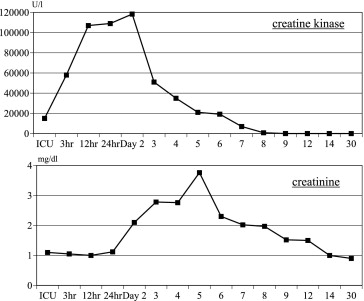
実際に突然の胸痛と左下肢麻痺を認めた大動脈解離の症例を提示する。術後にmyonephropathic metabolic syndromeに進展した。術後6日までは0.1μg/kg/minのスピードでhANPの投与を行い、その後漸減した。2日目にはCK濃度は118380U/Lにまで上昇したが、hANPの投与により、尿量は10,000ml確保でき、血清Creatinine値も5日目に3.76mg/dlをピークに血液透析を行うこともなくその後低下し、正常域にまで改善した。
下肢のチアノーゼ、腫脹、感覚異常、動作障害は徐々に改善し、30日後には後遺症もなく退院できた。
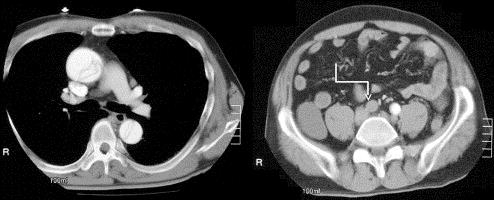
Preoperative computed tomography scan shows acute aortic dissection (arrow, right iliac artery)
http://www.annalsthoracicsurgery.org/article/S0003-4975(09)00356-7/fulltext
1999年にアルドステロン受容体拮抗薬の左室収縮機能低下心不全患者に対する予後と死亡率への影響を検討したRandomaized Aldactone Ebaluation Study:RALESの結果が報告された。
6か月以内にNYHAのClass Ⅳを呈したことがあり、エントリー時にⅢまたはⅣの1663例、左室駆出率35%以下のACE阻害薬とループ利尿剤で治療を受けている慢性心不全患者にスピロノラクトン追加投与とプラセボ群での比較試験である。
プラセボ群では372名(44%)の死亡に対し、スピロノラクトン群では283名(34%)の死亡が確認され、27%の死亡減少効果が認められた。非致死的再入院は、プラセボ群で764名(91%)、スピロノラクトン群で663名(81%)、入院はそれぞれ1317回と1088回で22%の入院減少効果を認めた。
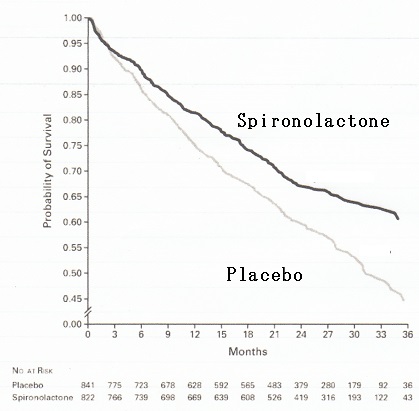
http://www.nejm.org/doi/full/10.1056/NEJM199909023411001
不安定狭心症に対して緊急CABGを行った154名の患者の長期世簿を規定する因子を検討した。手術死亡は1.9%、女性、慢性腎不全、血液透析、hANPの非使用治療、ARBおよびアルドステロン阻害薬の非使用治療、3か月後のBNP≧200pg/ml、3か月後のアルドステロン濃度≧100pg/mlが後の心イベントの危険因子であった。術中のhANPの使用、および、術後のARB及びアルドステロン阻害薬の使用により、レニンア・ンジオテンシン系の抑制が、心筋のリモデリングを予防し、更なる心筋梗塞を減少させ、心機能を改善させ、長期予後を改善したと考えられる。
http://www.ajconline.org/article/S0002-9149(10)00851-9/abstract
ACE阻害薬で治療を行っていても、アルドステロン値は治療当初は低下するが、その後次第に上昇してくる、エスケープ現象が認められる。
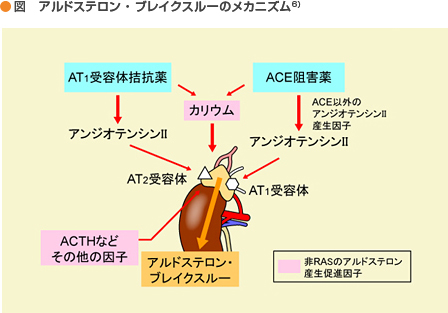
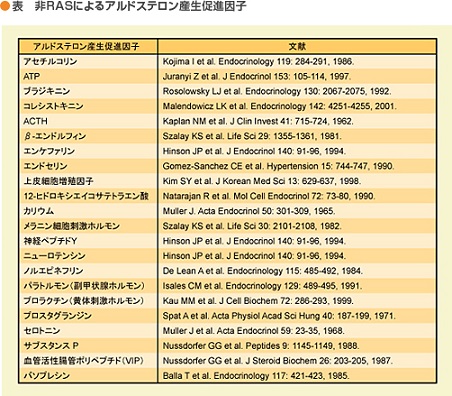
非RASを介したアルドステロン産生因子としては、RAS抑制によって上昇したカリウムに伴うアルドステロンの産生、ACTH、ノルエピネフリン、エンドセリン、セロトニンなどの様々な因子が想定されている。
Spat A et al. Physiol Rev 84: 489-539, 2004より一部改変
注)アルドステロン・ブレイクスルーの要因として、 1)非RASによるアルドステロン産生に加えて、2)不十分なACE活性阻害、3)非ACE経路を介したアンジオテンシンII産生(ACE阻害薬の場合)、4)アンジオテンシンIIのブレイクスルー、5)AT2受容体を介したアルドステロン・ブレイクスルーなどが考えられ、ACE阻害薬とARBとではアルドステロン・ブレイクスルーの要因が異なる可能性もある。
実際のアルドステロン・ブレイクスルー現象の頻度を調べた報告がある。
6か月以上の使用で10%以上、一年以上の使用で50%以上とも報告されている。
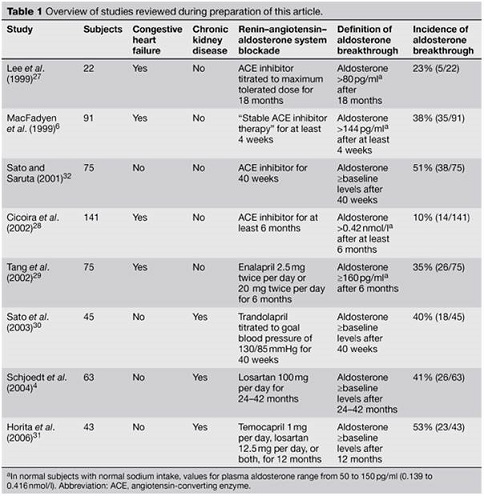
http://www.nature.com/nrneph/journal/v3/n9/full/ncpneph0575.html
ARBのCandesartanからOlmesartanへの変更で血圧を含めどのように変わるかを検討してみた。アンジオテンシン2もアルドステロンも、1年たっても減少したままであり、アルドステロン・ブレイクスルー現象はOlmesartanでは認められないと考えられる。
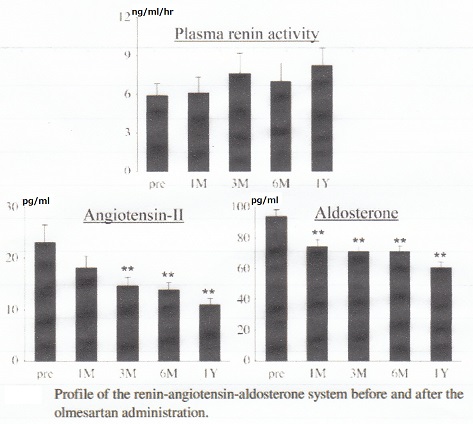
左室重量やBNPの値も低下したままである。
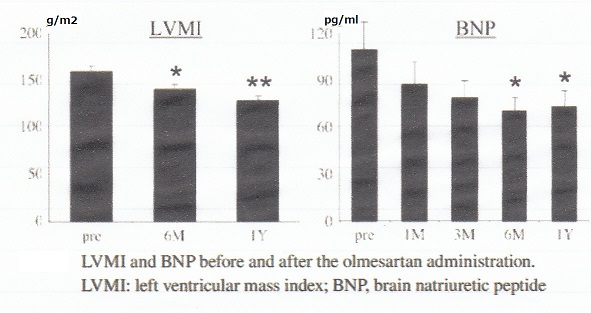
左室の重量とアンジオテンシン2は相関はないが、アルドステロンと相関があり、アルドステロンの低下を維持することが、心筋の肥大抑制になる可能性がある。
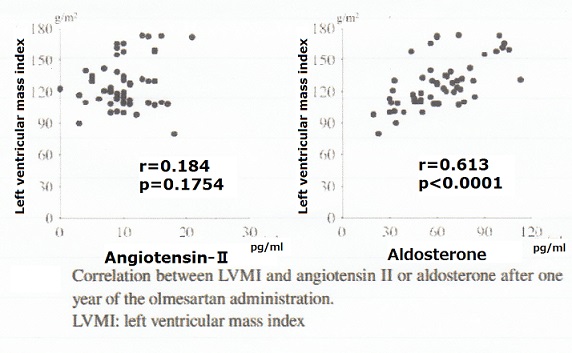
血圧もOlmesartanに変更後、一年たっても有意に低下していることが示された。
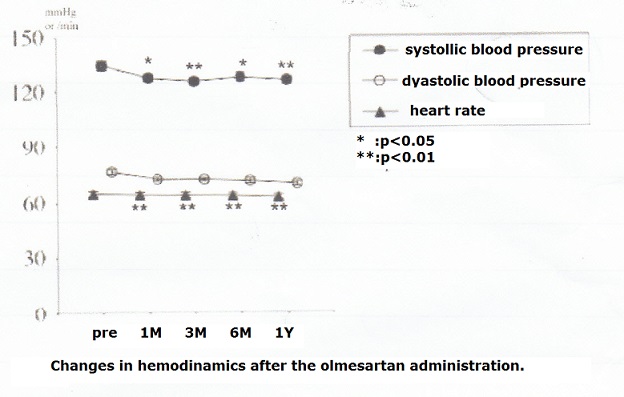
https://www.jstage.jst.go.jp/article/atcs/17/5/17_oa.11.01691/_pdf
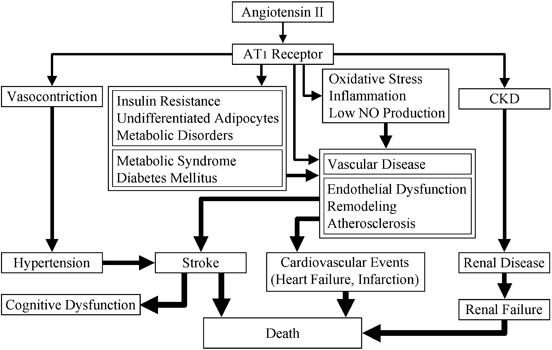
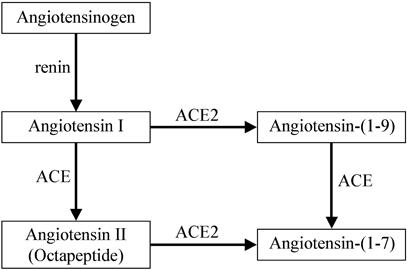
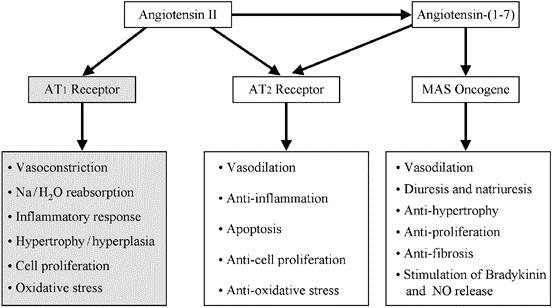
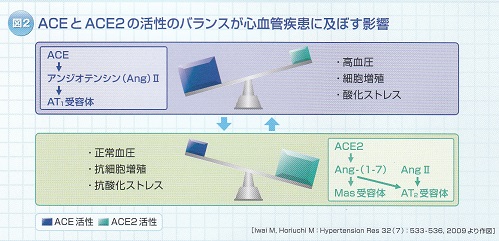
近年レニン・アンジオテンシン系はいろいろと新しい知見が構築されてきた。昇圧系として作用しているACE-angiotensin 2-AT1 receptor系と強力な昇圧物質であるアンジオテンシンの代謝物であるアンジオテンシン(1-7)とそれを代謝するACE2の系であるACE2-angiotensin-(1-7)-Mas receptor系は、逆の働きをする系として概念的に確立された。
http://www.nature.com/hr/journal/v32/n7/full/hr200974a.html