その他
2024.09.11
なぜ今、腹膜透析なのか? 藤井健太郎先生
2024年9月5日
演題「なぜ今、腹膜透析なのか?」
演者:けいゆう病院腎臓内科医長 藤井健太郎 先生
場所: けいゆう病院13階会議室
内容及び補足「
腹膜透析(Peritoneal Dialysis)とは、肝臓、胃、腸などの内臓表面や腹壁の内面を覆っている腹膜の中に透析液を一定時間入れておいて、を介して、血液中の老廃物や塩分、余分な水分などを移動させて、充分に透析液に老廃物や水分が移行した時点でこの透析液を体外に取り出す透析の方法。
CAPD(continuous ambulatory peritoneal dialysis):連続携行式腹膜透析とAPD(automated peritoneal dialysis):自動腹膜透析の2種類がある。
CAPD:1日に3から5回透析液を交換(バッグ交換)する。1階の交換にかかる時間早く30分。朝・昼・夕方・就寝前など生活のリズムに合わせて、基本的には患者本人や家族が透析液を交換する。
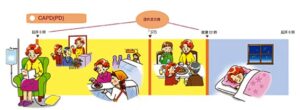
参:従来は2Lの1日4回のバッグ交換(朝、昼、夕方および就寝前)ではなく、少量の腹膜透析液(例えば1.3L)・低頻度(1日2,3回)のバッグ交換で始め、尿量、残存腎機能に合わせて透析量。回数を増やす「インクリメンタルPDの注排液」を採用する施設が多くなってきた。透析量が少ないと1回のバッグ交換は15分程度となる。
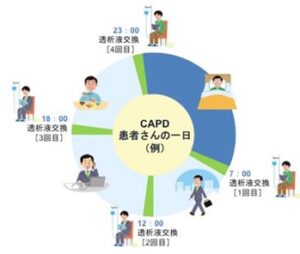

https://dialysis.medipress.jp/disease-and-cure/dialysis-basic/55
APD:主に寝ている時間を利用して透析液の交換を自動的に行う。現在約40%のヒトがこの方法を行っている。
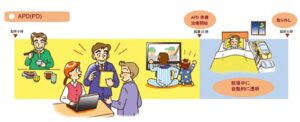
参:自動腹膜透析装置(サイクラー)を用いて透析液交換を行う方法で以下の2つの方法に大別される。

- NIPD(nocturnal intermittent peritoneal dialysis:夜間間歇式腹膜透析)
サイクラーを用いて、夜間のみ透析液の交換(3~6回)行う方法。ヘルニアやリーク(透析液の滲出)、腰痛などの合併症のある患者やCAPDで日中の腹部膨満感が強い患者に適している。しかし、小分子量の物質除去が不十分になりやすいため、実施は充分な残存腎機能がある患者に限る。尿量や残存腎機能の低下、データの悪化、尿毒症上の発言が心配される場合はCCPDへの変更を検討する。
- CCPD(continuous cycling peritoneal dialysis:持続周期的腹膜透析)
NIPDに、日中の透析液貯留を加えた方法。残存機能低下に伴い小分子の除去が不十分となった患者に用いられ、最も大きな透析涼の得られる方法。
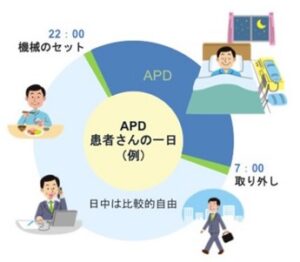
https://dialysis.medipress.jp/disease-and-cure/dialysis-basic/55
バッグ交換:腹膜透析液を入れている新しいバックを腹腔に注入し、老廃物や水分などを含んだ透析液をお腹から取り出す(排液)する作業。バッグ交換では、お腹から出ているカテーテルと新しい透析液が入ったバッグと廃液丁野からのバッグのセットを接続し、お腹の中の廃液を出した後、新しい透析液をお腹に入れる。その後、空になった透析液バッグと廃液で満たされたバッグをお腹から出ているカテーテルから取り外す。この接続・取り外し作業は、手動でも機械を用いて自動で行うこともできる(現在は約30%が手動、約70%が自動で接続作業を行っている)。
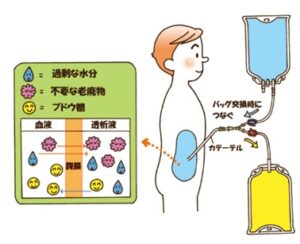
全国腎臓病協議会HP
https://www.zjk.or.jp/kidney-disease/cure/peritoneal-dialysis/dialysis-method/
参:
血液透析では血液を体外に採りだして血液の浄化を行うが、腹膜透析では、腹腔内に直接透析液を注入し、一定時間貯留している間に腹膜を介して血中の尿毒素、水分や塩分を透析液に移動させる。充分に移動した時点で透析液を大河に取り出すことにより血液浄化を行う。透析液は外気に触れることなく、通常は自然の落差を利用して透析液の交換を行う。注液時には新しい透析液バッグを腹腔より高い位置に置く。一方は家記事には空のバッグを腹腔より低くして透析液を排液バッグに取り出す。
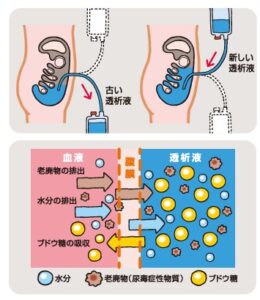
腹腔カテーテル:腹膜透析では手術により透析液の出し入れをするための腹膜透析カテーテルを腹腔内に埋め込む必要がある。腹腔カテーテルは長期的に使うので、腹腔カテーテルの出口部および周囲を清潔に保ち感染予防に努めることが重要。

https://jsn.or.jp/jsn_new/iryou/kaiin/free/primers/pdf/2022allpage.pdf
現在日本の透析患者の問題点
- クリニックに通えない
- 医療者が透析の場合つい血液透析を選択してしまう
- 透析患者の高齢化
があげられる。
本日は以下の三点について話す予定
- 透析患者の高齢化
- 腹膜透析治療デバイスの進歩
- SDMという概念の
日本では透析患者約35万のうち約1万人(約3%)が腹膜透析をしている。
世界では10万人が腹膜透析を行っていて、香港では約70%、カナダや欧州では20~30%、米国約10%である。
2022年末慢性透析療法を受けている患者総数は347474人、2022年に透析導入のうち血液透析は94.4%、腹膜透析は5.6%であった。
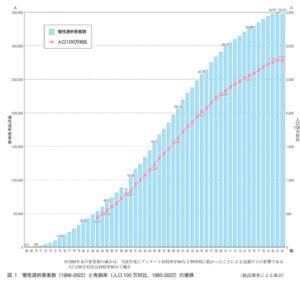
2022年日本透析医学会統計調査報告書 2022年12月31日現在
https://docs.jsdt.or.jp/overview/file/2022/pdf/01.pdf
問題は2000年の透析患者の平均年齢は61.2代であったが、2020年には69.4歳と高齢化してきている。現実に80から89歳でも透析を行っている。
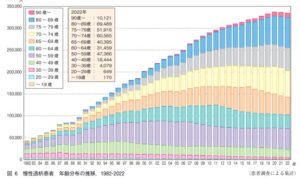
透析会誌56:473-536 2023
https://www.jstage.jst.go.jp/article/jsdt/56/12/56_473/_pdf/-char/ja
高齢透析患者の特徴および問題点として以下のものがある
ADLが低下している
食事量・骨格筋量が少ない
心疾患などの合併疾患のリスクが高い
抑うつ/認知機能の低下
免疫能の低下
参:高齢透析患者の臨床的特徴として、最も大きな問題は低栄養である。さらに運動機能の低下、慢性炎症などが、神経系の合併症や骨粗鬆症、付随する腎不全の合併症に影響を与えている可能性が指摘されている。
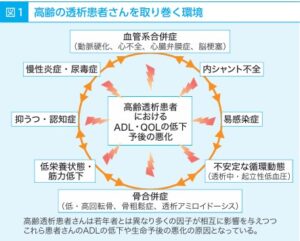
「高齢者にとって適切な腎代替療法の選択」兵庫医科大学病院倉賀野隆裕教授
https://baxterpro.jp/sites/g/files/ebysai771/files/2023-01/challenges_and_future_3.pdf
腹膜透析のメリットとして以下のものがある。
・通院回数が少ない
・体重に応じた透析量の調節が容易
・シャントによる心負荷や透析による血行動態変化が少ない
・導入後数年間の生命予後は腹膜透析が血液透析よりも優れている
・在宅で透析が行えるので流行感染からの隔離が可能(例Covid-19)
デメリットとしては以下のものがある。
・自分で行う負担、家族や医療者に手伝ってもらうという負担をかける
・介護施設では、法律上看護師以外の職員が透析を手伝うことができない
・開腹手術が必要である
・一連の手技(バッグ交換、出口部のケア)、トラブル時の対応の知識が必要
Assisted PD:身体および認知機能の低下によって自分で腹膜透析治療・管理ができない場合、家族や医療者からの支援を受けながら腹膜透析治療・管理を継続していく方法。
4589例の腹膜透析のアンケート調査によると患者自身が行っているのが90.3%であったが、PDの注排液を本人ができない場合に管理した介助者は、配偶者42.5%、子供36.0%、看護師15.0%であった。
腎と透析 86 (6) 793-797, 2019.
https://www.almediaweb.jp/diabetes_dialysis/diabetes_dialysis-002/part11/01.html
デイサービスを継続して利用した群でAssisted PDを継続して利用した8例と利用しなかった3例での1年間の検討ではあるが、継続して利用した群では、有害事象の発生はなく、安定したPDの注排液と在宅療養が可能であった。また、貧血や電解質採決結果、栄養状態に関しても、日本透析医学会が示す指標の基準値内であり、安定したコントロールが可能であった。
日本透析医学会の調査によれば、本邦における一年間の腹膜炎の発生率は14.5%であり、年齢が高くなるにつれて発症率が高くなる傾向があり、平均年齢が78.5±6.4歳という高齢者の対象が、1年間大きなトラブルなくPDの注排液療養を継続できたことはデイサービスによるAssisted PDのこうかを示唆する結果であるとか案が得る。
透析会誌52(7):433~441,2019
https://www.jstage.jst.go.jp/article/jsdt/52/7/52_433/_pdf
参:高齢者におけるCAPDのメリットとデメリット

透析会誌 50(11)677-383 2017
https://www.jstage.jst.go.jp/article/jsdt/50/11/50_677/_pdf/-char/ja
参:腎代替療法の比較表
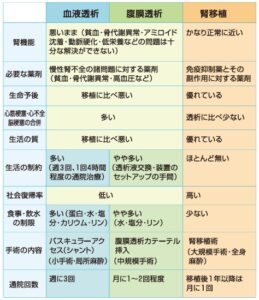
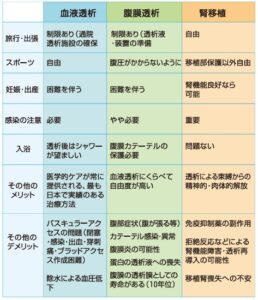
腎不全:治療選択とその実際 2022年版
https://jsn.or.jp/jsn_new/iryou/kaiin/free/primers/pdf/2022allpage.pdf
カテーテル挿入術
腹膜アクセス手術の善し悪しがその後のPD管理に直結する重要な因子となる。現時点で(2019年のガイドライン)で留置法の優劣を示すエビデンスとなるRCTはない。
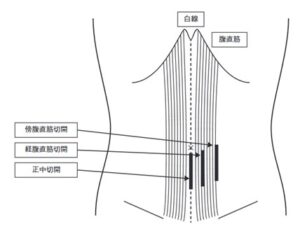
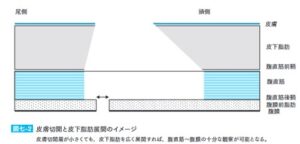
腹腔内に外科的に入るためには、通常の外科手術での開腹術では腹部正中切開により白線直上を切開して入ることが多い。筋肉や下腹壁動静脈に伏せずに手術ができるからであるが、PDカテーテル挿入に際しては敬服直近切開での挿入術が望ましい。根拠の一つ目は、カテーテルを腹壁に寝かせて挿入するためにカテーテルを複直筋前鞘の下に挿入することが重要であるが、これは敬服直筋切開でしかできない。二つ目は皮下トンネル感染症が生じた際に、血流が豊富な複直筋内部を貫いている場合、感染防御因子(白血球やグロブリン、抗生剤など)が供給されやすく、感染に強いことが期待できるからである。
カテーテル関連感染=「腹膜透析カテーテルの組織通過部分の外周囲における病原体感染」
・出口部感染:皮膚発赤の有無にかかわらず出口からの膿性浸出液が認められる状況
・皮下トンネル感染:皮下トンネル部に沿って臨床的な炎症所見あるいは、超音波検査による液貯留が認められる状況
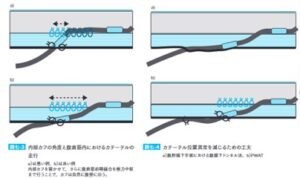
カテーテル関連感染が維持期の腹膜透析患者に発症する場合、その行減退感染経路は原則として出口部→皮下トンネル周囲→外部カフ→内部カフと考えられ、感染が内部カフに至ると腹膜炎に進展する。なお、皮下トンネル付近の掻破巣からカテーテル周囲への感染波及など、出口部感染を経ない感染進展も起こりえる。
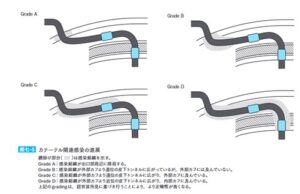
代表的な皮膚常在菌である表皮ブドウ球菌に限らず、グラム陽性球菌からグラム陰性桿菌、コリネバクテリウム、ジフテロイド、迅速発育抗酸菌、真菌など様々な病原体がカテーテル感染の原因菌となり得る。我が国の小児PDの注排液礼を対象にしたアンケート調査では、出口部・皮下トンネル感染の起因筋のうち59%が黄色ブドウ球菌(20%がMRSA)であり、MRSA腹膜炎の55%に皮下トンネル感染を伴っていたとの報告がある(Pediatr Nephrol 2006 21 28-34)。
腹膜透析ガイドライン2019
カテーテルの先端は特徴と膀胱の間にあるダグラス窩に留置する。
出口部位決定のポイントとして以下のものがある。
- 挿入部位とカテーテル出口部が日常生活に支障がない
- 出口部ケア(洗浄や消毒)がしやすく直視可能
- ベルトや衣服に圧迫されない
- 体位変化(仰向け、座位、立位)による支障がない
- 腹部の手術痕以外の場所
- 入浴パックが装着可能な位置
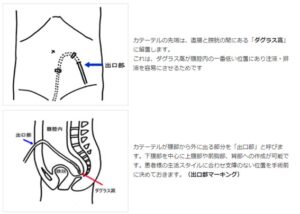
カテーテルの材質はシリコンで、注排液がスムーズに行えるように先端部の10cm範囲内に多数の側孔がある。中間には、下付と呼ばれるダクロンフェルトがあり、外部カフは皮下に固定し、内部カフは複筋膜に固定するとこで組織と融合される。
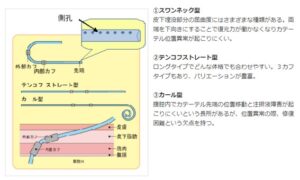
待機的に中部を挿入するSMAP(Stepwise initiation of PD using Moncrief And Popovich)法が行われるようになった。
必要な時期に透析が開始でき、埋没期間中に手術創が治癒することで感染症などが起こりにくくなるし、計画的に透析導入が行えるだけでなく入院期間が短縮できる利点がある。
https://www7.kmu.ac.jp/keihanpd/pd_basic_knowledge/4-3/
腹膜透析の進歩
17世紀から腹腔を穿刺して腹水症の治療が行われており、19世紀後半になり腹膜の代謝輸送過程に関する動物実験、水分除去に腹膜を利用する原理の発見、腹膜における溶質移動と腹腔内へ注入された高張液が限外濾過に与える研究などが進んでいた。
1923年にPutnamにより腹膜の溶質移動、拡散および浸透に関する包括的研究が行われ、溶質移動は、拡散、濃度勾配を用いた物質移動によると報告され、Ganterはヒトの急性腎不全患者に対して初めて生理食塩水を腹膜透析液として、腹膜透析療法を実施された。この頃は一方から注入し、他方から流出させる持続的透析法が用いたられたが、水分バランスがとりにくく、腹膜炎を合併しやすかった。
1946年Abbottらにより間歇咳腹膜透析法が提唱され、1948年にFrankらは、間欠的腹膜透析法の連続使用のために、重炭酸を緩衝液に使用し20Lタンクの腹膜透析液の方法を示した。
1950年にOdelらは透析液やカテーテルを工夫し、自動的な注排液を可能とするシステムAPDを開発した。
1968年Tenckhoffらによりシリコン・ラバー材の腹膜透析カテーテルが開発された。
1976年4月のアメリカ臓器学会の抄録集に「The definition of novel portable/wearable equilibrium peritoneal dialysis technique」というえんだいがPopovich, Moncriefらにより2Lの透析液を1日5回交換することで、尿素窒素やクレアチニンなどの除去が可能であったと発表された。
我が国では、1980年よりCAPDのメリットが導入され、1984年在宅でのCAPDのメリット健康保険適用、施設基準が設定された。

透析会誌 50(11)677-683 2017
https://www.jstage.jst.go.jp/article/jsdt/50/11/50_677/_pdf/-char/ja
透析液の変遷
1983年に日本でPDが導入された際には、透析液はpH 40.5~5.5程度の産生であった。生体適合性の面からは透析液は中世が望ましいと考えられていたが、当時は浸透圧付加剤であるブドウ糖はpHが中性領域に近づくにつれ不安定となり、分解が起きてGDPs(glucose degradation products)が産生されてしまうため、産生にせざるを得なかった。その上、加熱滅菌時に大量のGDPsが産生され、腹膜障害の大きな理由として報告されていた。さらに、一部のGDPsであるカルボニル化合物はタンパク質のアミノ基と非酵素的に反応し、AGEs(advanced glycation end-products)となり、一層腹膜障害を起こし腹膜機能低下が起きることが示されていた。また、酸性液の使用により、細胞内pHの低下によって中皮細胞や線維芽細胞などに障害を与えることも報告されていた。このような障害は被嚢胞性腹膜硬化症(encapsulated peritoneal sclerosis:EPS)の発症要因となった
2000年になり、酸性のブドウ糖液とアルカリ性の電解質液を隔壁で分離した中性透析液が登場した。このバッグは使用時に隔壁を開通させて混合し中性化を図るものである。これにより、中性か並びに低GDPsを実現することが可能となった。
人工臓器46 63-66 2017
https://www.jstage.jst.go.jp/article/jsao/46/1/46_63/_pdf
2018年に腹膜透析分野において国内初めてのクラウドベース通信プラットフォームであるシェアソース(腹膜透析用治療計画プログラム)が発売され、PDの注排液治療においての遠隔患者管理が開始された。
2022年には診療報酬改定にて遠隔モニタリング管理加算が新設された。
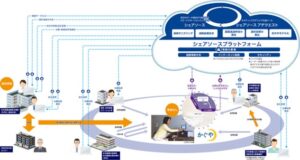
https://baxterpro.jp/kaguya/sharesource_roundtable_meeting
BaxterからホームPDシステムかぐや(自動腹膜寒流装置)

https://baxterpro.jp/products/pd/kaguya
Terumoから自動腹膜寒流装置マイホームぴこ
https://www.terumo.co.jp/medical/equipment/me144.html
https://www.terumo.co.jp/medical/equipment/md/upload_files/470034_21300BZZ00199000_B_02_04.pdf
などが発売されている。
腹膜透析の遠隔モニタリング機器として、JMSが開発したのがAPD装置PD-RelaxaおよびRelaxaリンクである。体重計、血圧計、体温計のデータをBluetoothで取り込み、自宅でAPD装置を利用してPDの注排液を行いながら医療機関と連携することが可能となる。
PD-Relaxaを起動すると、大型ディスプレイに医師からの連絡が表示される。それを確認了解するとAPD装置が動き出す。機器のセットアップは自動で行われ、薬液都会をロつなげると治療の準備が完了する。APD療法は注液、排液はすべて自動で、何かが起きるとアラームが鳴って知らせてくれる。APD治療が終わると、体重計、血圧計、体温計のデータをBluetoothで取り込み、治療データとともに主治医の元に遠隔通信システムを介して送られる。バッテリー搭載で、緊急時にもバッテリーで対応できる仕組みである。
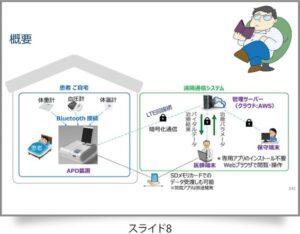
PDの注排液セミナー腹膜透析の遠隔モニタリングのこれから
https://medicalcapd.jms.cc/interview/seminar/001.html
PD Doctor’s EyeはMETRiCAが開発した腹膜透析患者が在宅で安心して診療を受けられるオンライン診療情報通信機能を備えた遠隔管理システムである。

https://pd-doctors-eye.metrica.me/
行動意思決定Shared Decision Making:SDM
「質の高い医療決断を進めるために、最善のエビデンスと患者の価値観、好みとを統合させるための医療者と患者間の協働のコミュニケーション・プロセス(Spatz ES JAMA 2016)」「患者と医師が情報、直感だけでなく決定を下すことも共有する協働的な努力・企て(Whitney SN Ann Intern Med 2003)」「医療者と患者が協働して医療上の決定を下すプロセス(Legare F Patient Education and Counseling 2014)」と、各論文に記載されている通り、医学的な情報や最善のエビデンスと、患者の生活背景や価値観など、医療者と患者が、双方の情報を共有しながら、一緒に意思を決定しているプロセス。
治療方針決定の代表的なアプローチには、「パターナリズムpaternalistic approach」、「インフォームドアプローチ informed approach」、「協働アプローチ shared approach」がある。
パターナリズムでは、過去の経験や最新の知見に基づき医療者が意思を決定する方法。
インフォームドアプローチでは、医療者が患者に選択し・情報を提示し、患者が自己責任で意思を決定する方法。
協働的アプローチでは、医療者からの情報とともに、患者からの情報も含め、患者のニーズに基づき話し合いを重ねて協働で意思を決定する方法。
治療の有効性が明らかで、合併症のリスクが少なく、放置した場合に生命の危険が高く、迅速な決断が要求される場合にはパターナリズムが妥当と考えられる。
一方、唯一最善那智療法が明確でなく、治療法に選択肢がある場合にはインフォームドアプローチがとられることになると考えられるが、患者や家族にとって、提供された情報を正しく決定することは有意ではないことも少なくないので、SDMが適切であろうと考える。特に腎代替療法の選択に関してはSDMが適切だと考える。

SDMで、医療提供者と患者が最善のエビデンスに基づき、最善の治療法を一緒に選択していくためには以下のようなプロセスをとる。

https://www.ckdsdm.jp/sdm/sdm.html