川村所長の勉強会参加記録
2023.07.14
ARNIをどうやって使う? 木原正夫准教授
2023年7月7日
演題「腎臓内科医からのSuggestion、ARNIをどうやって使う?」
演者:順天堂大学大学院医学研究科 腎臓内科学講座 准教授 木原 正夫 先生
場所:
内容及び補足「
症例提示
84歳女性:タンパク尿 0.15g/gCr以下(定性:陰性)、オルメテック10㎎、メインテート5㎎、スピロノラクトン25㎎、アゾセミド60㎎、ベラパミル240㎎、アロプリノール100㎎、ワーファリン2㎎、ラベプラゾール5㎎粗放していてCr 1.00→3.28に上昇した。血圧を見てみると110→90mmHgと低下していた。この状態で紹介されたが、ここで悩むのは、腎機能が悪化しているのでRAS阻害薬をやめるか、心・腎保護を考えるとRAS阻害薬は続けたいが・・・。と悩むことになる。
実際のCKD診療ガイドライン2013年ではどうなっているかというと、糖尿病を合併しているかどうか、蛋白尿の呈しているどうか、で高血圧の治療目標が分類され、糖尿病の合併を認める患者蛋白尿を認める患者は、130/80未満が目標にされている。腎機能が悪い場合には、カルシウムブロッカーが推奨されている。
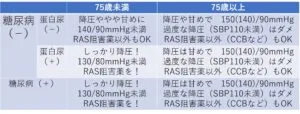
https://jsn.or.jp/guideline/ckdevidence2013.php
高血圧治療ガイドライン2019でも、判断基準の中に、糖尿病の有無、蛋白尿の有無、高齢者か?動脈硬化が存在するか?という判断が求められる内容となっている。

http://www.hcc.keio.ac.jp/ja/research/assets/files/b78ce35fc55aef694ff6d4edbcd1143d.pdf
個々の症例に個別化して考えることが必要となってくる。
高血圧が腎機能の障害の原因となっているが、血圧が急に上昇しても腎機能はある一定期間保たれている。
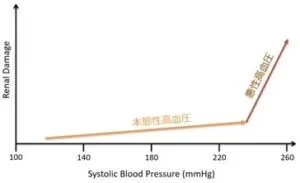
この理由は、健常人においては、ある程度血圧が上昇しても腎臓への血圧や、腎血流、糸球体静水圧は変わらない。
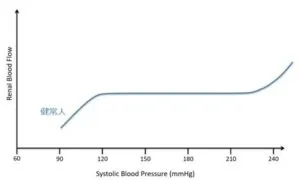
Hypertension. 2004;44:595-601.
https://www.ahajournals.org/doi/pdf/10.1161/01.HYP.0000145180.38707.84
その機序は、GFRのオートレグレーションによる。輸入細動脈の抵抗、輸出大動脈の抵抗をコントロールして腎臓を灌流する動脈圧、GFRを維持している。
輸入細動脈の抵抗は、筋原反応、尿細管糸球体フィードバックが大きく関わり、輸出細動脈の抵抗はアンジオテンシン2が大きく関わっている。
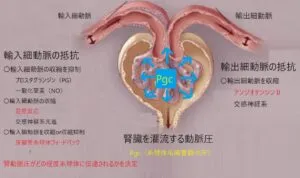
高血圧の時の血圧が上昇しても、輸入細動脈が収縮して、糸球体毛細血管静水圧とGFRの大きな変化を抑えて、腎臓へのダメージを減らし、腎障害が徐々に進行することとなる。
さっきの症例のように血圧が低下するとどうなるかというと、輸入細動脈が拡張して、腎臓に血流をしっかり入れ、輸出細動脈の抵抗を上昇させ、糸球体の圧を上げて、血圧が低下しても糸球体毛細血管静水圧とGFRの変化を抑える。
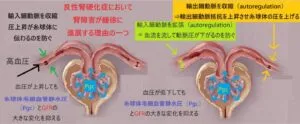
さっきの症例でなぜCrが上昇したのかを考える。
腎臓のオートレグレーションによる糸球体濾過量を維持する機構はどんな時でも有効に働いているのか?と考えてみよう。
CKDの時には自動調節機能が有効に働いていない。
参:血圧の上昇に伴い、健常者(A)においては腎臓の血管の圧自動調節能により腎臓の血流は一定に保たれる。片側腎になるとB、糖尿病の合併やCKDの合併の場合にはC、腎臓の圧の自動調節能の5/6が喪失するとDの変化になる。
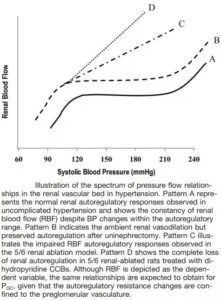
Hypertension. 2004;44:595-601.
https://www.ahajournals.org/doi/pdf/10.1161/01.HYP.0000145180.38707.84
CKDの腎障害の機序として二つのCommon pathwayがある。一つが糸球体高血圧で、もう一つが腎虚血である。
糸球体高血圧はネフロンロスによりシングルネフロンに対する圧が上昇し、糸球体高血圧になる。その結果蛋白尿が出現する。
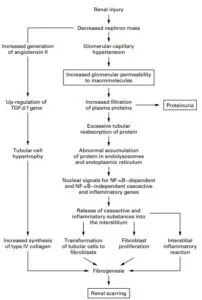
NEJM 1998 339 1448-56
https://www.nejm.org/doi/10.1056/NEJM199811123392007
腎虚血は、糸球体硬化(C)が起こり輸出細動脈以降の血流が悪化する(D)ため、毛細血管網の消失→間質の線維化→酸素拡散の減少(A,B)が出現するが、の変化の際には、あまり蛋白尿は認めない。
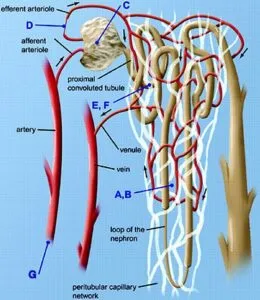
Journal of the American Society of Nephrology. 17(1):17-25, January 2006.
この二つの変化を臨床的にみられるのが糖尿病性腎症である。
2011年1月から2913年12月までの間に腎代替療法を受けた日本人患者(糖尿病性腎症50齢、腎硬化症50齢)の臨床軌跡の違いをeGFR、尿中アルブミン/Cr(UACR)で比較した。
糖尿病性腎症症例は青い点・線、腎硬化症症例は黄色の点・線で示している。糖尿病成人症症例はアルブミン尿が増悪し、その後腎機能が低下していく経過を呈している。腎硬化症症例は、アルブミン尿の増悪もそれほどでなく、腎機能も徐々に悪化している経過をとっている。
糖尿病性腎症の経過(糸球体高血圧の青線)
1 早期に過剰濾過
2 微量アルブミン尿を呈する
3 顕性蛋白尿を呈する
4 腎機能低下
腎硬化症の経過(腎虚血の黄色線)
1 早期に過剰濾過なし
2 蛋白尿は陰性
3 腎機能低下
4 CKDステージが進んでくると蛋白尿が軽度増加
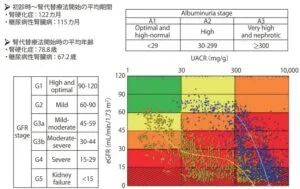
J Diabetes Res. 2016;2016:5374746
高血圧患者22例の腎生検と血圧正常の高齢者で腎疾患で外科的手術で得られた8例の腎臓の病理所見を正常の糸球体、肥大した糸球体、委縮した糸球体で比較してみる。
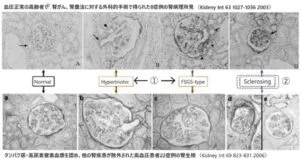
肥大した糸球体の問題は、糸球体が肥大しているので糸球体内圧が上昇しているので輸入細動脈が収縮して糸球体内圧の上昇を下げたいが、筋原性反応の機能不全があり自動調節脳が破綻している状態となっているので、体血圧の上昇により、糸球体は肥大し、糸球体高血圧となっている。この時点で輸入細動脈を見てみると、内腔を閉塞していないが、病理学的には硝子様変化が認められる。この硝子様変化が筋原反応を低下させていると考えられる。
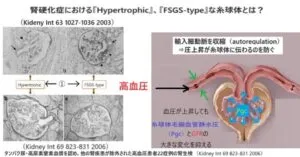
腎硬化症の状態である輸入細動脈が高度に狭小化しており、自動調節脳も破綻している状態である。この高度に狭小化している状態では体血管圧は糸球体には届かず、糸球体は委縮してしまい、糸球体内圧・血流も低下し虚血の状態になる。輸出細動脈はレニン分泌亢進により収縮して、糸球体内圧を保とうとしているが、RAS阻害薬が処方されている症例が多く、糸球体内圧を保ちにくい状態になっている。
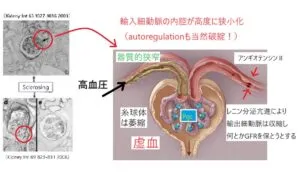
加齢、高血圧、糖尿病、脂質異常症、高尿酸血症、喫煙などの動脈硬化危険因子が背景にあり、細動脈の動脈硬化が進行し、自動調節機能不全が出現する。この機能不全は糸球体高血圧と糸球体虚血の二つの機序からCKDが進展することが考えられる。
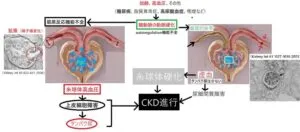
Kidney Int. 2003 63:1027-36
https://linkinghub.elsevier.com/retrieve/pii/S0085253815489719
Kidney Int. 2006 69:823-831
https://linkinghub.elsevier.com/retrieve/pii/S008525381551569X
CKD進行抑制のためには何が必要か?
腎障害とアルブミン尿は、全死亡、心血管病死亡と関連している。
一般住民105872名を対象とした14コホート研究のメタ解析の結果では、腎機能はeGFR 60 ml/min/1.73m2未満で心疾患、全死亡のリスクとなり、さらにGFRが低下すればするほど相対リスクは高くなったまたアルブミン尿・タンパク尿も腎機能とは独立した心血管疾患、全死亡の危険因子であり、アルブミン尿・タンパク尿の増加に従って、心血管疾患、全死亡のリスクが高くなることが示された。
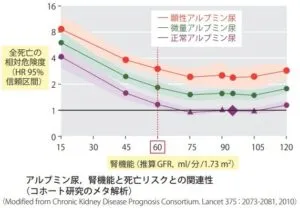
Lancet 375 2073-2081, 2010
https://www.jstage.jst.go.jp/article/naika/105/5/105_802/_pdf
蛋白尿減少率が上がれば、末期腎不全のリスクが低下する。
参:1094人の高血圧を有する腎疾患患者で中央値3.8年の経過を見た。ベースラインの蛋白尿はGFRが低いほど多かった。
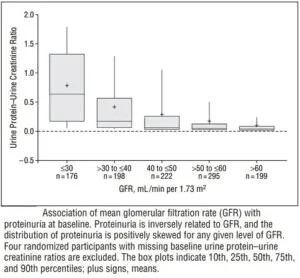
GFRの傾きは、特定のベースラインGFRでタンパク尿の程度が増加するにつれて急になった。
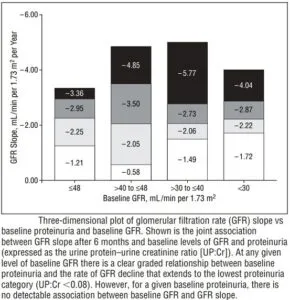
ベースラインから6か月後までの蛋白尿の変化とESRDの相対危険度が正の相関を示した。
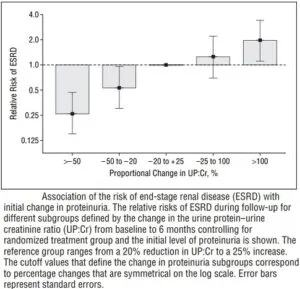
Arch Inter Med 2005 165 947-953
https://jamanetwork.com/journals/jamainternalmedicine/fullarticle/486515 file:///C:/Users/jeffbeck/Downloads/ioi40514.pdf
RAS阻害薬を使用してアルブミン尿が減少すれば、腎エンドポイント発生リスクが低下する。
参:2型糖尿病、高血圧、一般集団におけるアルブミン尿の程度によりeGFRの低下速度は異なるが、アルブミン尿の程度が強いほどeGFRの低下が大きい。
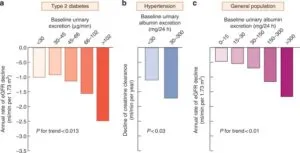
アルブミン尿が多いほど末期腎疾患:ESRDになる相対リスクが上昇する。
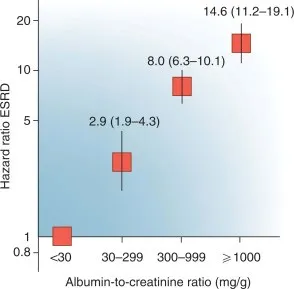
アルブミンが糸球体壁を通過すると、キュービリン-メガリン複合体のために尿細管細胞に再取り込みを受ける。アルブミンは、炎症、線維症、メサンギウム拡大、高血圧につながる一連の病原性メカニズムを引き起こし、最終的に進行性腎機能障害を引き起こす。細胞外シグナル調節キナーゼ(ERK)、核内因子-κB(NF-κB)、プロテインキナーゼC(PKC)の活性化及び炎症性タンパク質-1(MCP-1)、RANTES(活性化されたT細胞から分泌されるケモカインCCL5)、血管活性酸素種(ROS)、エンドセリン、TGF-β、コラーゲンなどが不可逆的な腎障害を引き起こす。
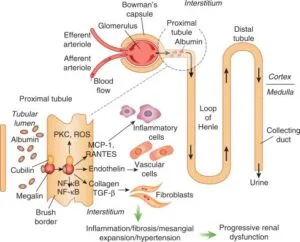
Kidney International 2014 86 40-49
https://www.sciencedirect.com/science/article/pii/S0085253815302519
一方で、AASK研究でアフリカ系の腎硬化症で蛋白尿がほとんどない人で、降圧薬としてCCBであるAmrodipineを使用した症例に比べ、ACEIであるRamiprilを使った症例でGFRが早く低下する。さらに、通常降圧をするよりも厳格降圧する群で早くGFRが低下することが示されている。
つまり、蛋白尿がない虚血主体の病態では、RAS阻害薬の使用や厳格な降圧が腎障害の進展を促進させるリスクがあると言える。
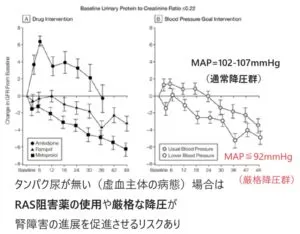
参:高血圧のアフリカ系アメリカ人1094名で平均動脈圧を通常の102~107mmHgを目標とした554例と、92mmHg以下を目標とした540例で約4年経過を見た。
治療開始から6か月後には、アムロジピン群では58%蛋白尿は増加したが、メトプロロール群では14%減少した。同じ期間で、タンパク尿は、通常血圧治療群では7%の増加、厳格治療群では17%の減少を示した。
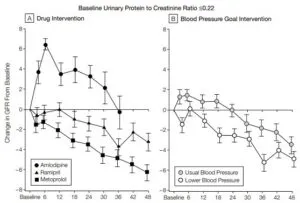
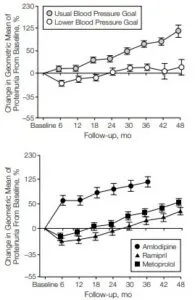
JAMA. 2002; 288: 2421-31
https://jamanetwork.com/journals/jama/fullarticle/195530
実際に降圧療法をどうするか?
糸球体高血圧の症例においては、Cr値は多少上昇していても、腎臓サイズは、正常だったり、腫大したりしており、その場合の降圧療法は、輸入細動脈の自動調節脳は低下しているが、厳格降圧が推奨され、その上、RAS阻害薬を併用することにより輸出細動脈を拡張させ、糸球体内圧を正常化し、腎保護を目指す。
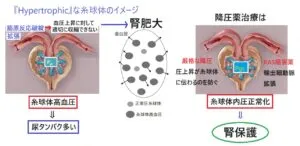
萎縮した腎臓の場合には、画像を見ても委縮した腎臓であることが多く、輸入細動脈は、器質的狭窄があり、腎血圧低下に対して適切に拡張できず、厳格な降圧すると糸球体に還流する動脈圧はさらに低下し、そこにRAS阻害薬を使うと輸出細動脈が拡張し、糸球体内圧が高度に低下し、さらなる腎機能悪化を招くことになる可能性がある。腎虚血の症例の場合には降圧に関しては、個別に気を使う必要がある。
先ほどの症例は、腹部CTで、腎臓は委縮していたので、虚血した糸球体が多そうなので、過度の降圧で悪化したと考えられ、循環器内科医と相談し、RAS阻害薬を中止し、血圧110-120mmHgに上昇し、Crは1.5前後に改善した。
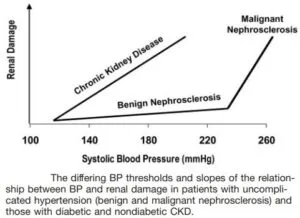
参:腎予後の観点から、腎硬化症は良性腎硬化症と悪性腎硬化症に分けられてきた。しかし、両性腎硬化症であっても末期腎不全に至るリスクはある。
高血圧患者全体として考える場合末期腎不全発症率は極めて低いものの、高血圧患者数が圧倒的に多いために末期腎不全の原因疾患としては三番目に重要な疾患であるし、それ以外の病態の合併の状態により、腎臓の悪化速度が異なってくる。
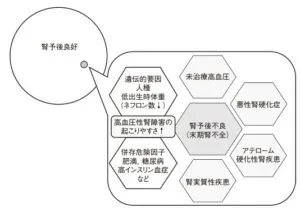
血圧レベルと腎障害の起こりやすさは、病態によって異なることが知られている。
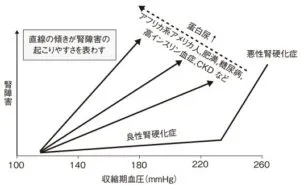
良性腎硬化症では、血圧レベルが悪性高血圧症のようによほど上昇しない限り、腎障害はほとんど起こらない。その背景に本態性高血圧の高血圧発症機序が密接にかかわっている。
本態性高血圧患者では輸入細動脈の血管抵抗の上昇に関連した末梢血管抵抗の上昇が高血圧の発症に関与していると考えられているが一方で糸球体から見ると、輸入細動脈の血管抵抗上昇は全身の高い血圧が糸球体に直接伝わらないように保護的に働くことになる。
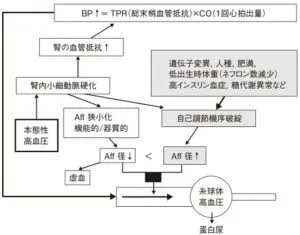
これに対して糖尿病性腎症などのその他の慢性腎臓病の患者では、わずかな血圧レベルの上昇が腎障害の進行に容易につながる。このような血圧による腎障害のsusceptiblityの亢進に糸球体血圧の自己調節機序の破綻、特に筋原反応の障害が関与していることが示されている。腎内細動脈硬化症は最終的に自身が灌流する糸球体に効果病変を引き起こすが、糸球体効果病変には虚血に関連した硬貨病変と糸球体高血圧に関連した硬貨病変の二種類が存在することが示唆されている。フランスの病理学者Hillらは形態的な検討から、輸入細動脈にみられる硝子化病変が高度で内宮の狭小化を伴う場合は虚血性障害を、一方軽度である場合は、自己調節機序の破綻に関連して糸球体高血圧をもたらしている可能性があるk十を報告している。一般的には虚血に関連した機序が腎障害の主たる病態機序だと考えられているが、より腎障害が進行しやすいアフリカ系アメリカ人の本態性高血圧患者では糸球体高血圧に関連した硬貨性病変の割合が、コーカシアンに比べて高いことが知られている。実際African American Study of Kidney Disease and Hypertension(AASK)では、肥満合併例では血圧レベルの上昇に伴い蛋白尿の増加が見られ、より腎障害進展リスクが高かったことが示されている。
一方で糖尿病患者では、非糖尿病患者に比し、血圧レベルの上昇に伴うアルブミン尿の増加が比較的正常なレベルの血圧時から見られ、130mmHg以上で急峻に上昇することが大規模な疫学研究結果でも示されている(Hypertension 2015;65:510―516)。
糖尿病患者では細動脈硬化に関連して糸球体血行動態調節機序の破綻から糸球体高血圧を招くことがよく知られており、血圧依存性腎障害のsusceptibility亢進に寄与すると考えられている。これまでのところ、遺伝子変異、人種、低出生時体重(ネフロン数減少)、糖代謝異常や高インスリン血症の合併が本態性高血圧患者の腎障害進展を加速させている重要な因子であると考えられている。
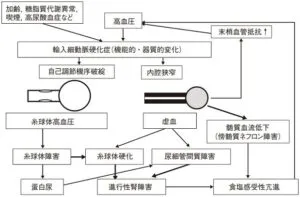
JSH2014高血圧治療ガイドラインでは、蛋白尿がない場合の降圧目標を140/0mmHg未満、使用薬剤はCa拮抗薬、RA阻害薬、利尿薬を、一方でタンパク尿が0.15g/gCr以上で降圧目標は130/90mmHg未満で第一選択薬としてRA系阻害薬の使用が推奨されており、糖尿病合併例と同様な内容になっている。
腎硬化症による腎障害の進展機序は虚血と糸球体高血圧の二つの糸球体血行動態異常であり、その背景には2つの異なる輸入細動脈硬化症の存在があることから、全身血圧と輸入細動脈病変の特性の2つの因子によって糸球体障害が規定される。
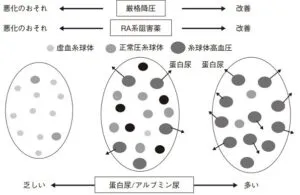
治療上重要なことは、これらの2種類の糸球体血行動態異常が1個の腎臓に様々な割合で巣状に分布し、病態や患者ごとにその割合が異なる点である。
下図の右側のように、糸球体高血圧主体の病態においてはより厳格な降圧が求められ、輸出細動脈を拡張し糸球体血圧低下により有効と考えられるRA系阻害薬が第一選択薬として合理的な選択だと考えられる。一方で下図の左側に示すように蛋白尿に乏しい虚血主体の病態においては過度な降圧やRA系阻害薬の使用は腎障害の進展を促進させてしまう恐れがあると考えられる。
臨床的に判断する場合には、尿タンパクが多い場合は糸球体高血圧主体の病態を、一方尿タンパクが陰性である場合は虚血の病態を念頭に置く必要がある。特に高齢化が急速に進行しつつある我が国においては、潜在的な高度腎内小細動脈病変を有する場合が少なくない。タンパク尿が陰性で血圧コントロールが悪くないにもかかわらず進行性にeGFRの低下が見られるような症例では、虚血の病態を念頭に降圧目標を上方に設定したり、RA系阻害薬の減量や中止、Ca拮抗薬への変更などを考慮したりする必要がある。
日腎会誌 2016;58(2):85‒91
https://jsn.or.jp/journal/document/58_2/085-091.pdf
CKD診療ガイドライン2023の第2章 高血圧・CVDの降圧の推奨薬は、糖尿病の有無にかかわらず、蛋白尿の有無を参考に検討するよう推奨されている。

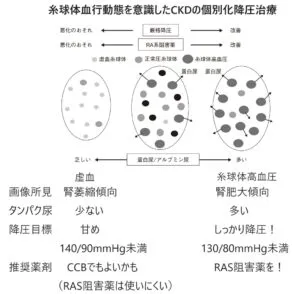
まとめると、画像で腎臓の萎縮傾向の症例では蛋白尿が少なく、こういった症例では腎虚血になっていることが多く、RAS阻害薬が使いづらく、降圧は甘めでCCBの輸入細動脈を開く薬でいい。画像上で腎腫大傾向が多い症例では、蛋白尿が多く、糸球体高血圧をイメージし、しっかりした降圧が必要であり、RAS阻害薬を優先的な使用を考える。
実際には糸球体の肥大状態は、腎生検を行わない限りわかないので、実臨床では、RAS阻害薬を使用したら、自分の想像以上にCrが上昇したら、虚血の糸球体が多いと考え、RAS阻害薬からCCB変更を考慮する。
実際Crが上昇した症例で、RA系阻害薬の中止で腎機能の改善や悪化の阻止が可能か?
重症の進行性CKD患者(CKD G4/5)におけるRAS阻害薬中止がeGFRを改善もしくは安定化させるかを検証した(411例で3年間:平均年齢63歳、ベースラインの蛋白尿1.018g/gCr)トライアルでは有意な差は認めなかった。
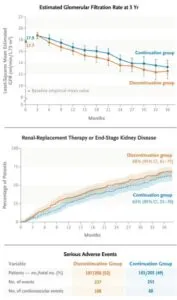
N Engl J Med. 2022 Dec 1;387(22):2021-2032.
https://www.nejm.org/doi/10.1056/NEJMoa2210639
同じ重症の進行性CKD(CKD G4/5)(52例:平均年齢71歳、ベースラインの蛋白尿0.68g/gCr)のACEi/ARBを投与している患者に対してタンパク尿や腎機能の変化を検討した観察研究では、患者の61.5%はACEi/ARBが中止されてから25か月後にeGFRが12%以上増加した。これは24か月まで持続した。
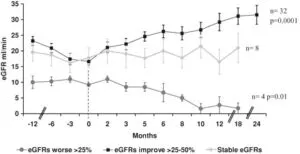
Nephrol Dial Transplant 2010, 25 3977–3982,
https://academic.oup.com/ndt/article/25/12/3977/1862962
両研究の違いは、平均年齢63歳、ベースラインの蛋白尿1.018g/gCrと平均年齢71歳、ベースラインの蛋白尿0.68g/gCrで差があり、改善した分では糸球体の虚血がある症例が後者の研究で多かったという推測ができる。
観察研究では、RAS阻害薬を中止後、腎機能悪化は抑制したが、心血管イベントは増加したとする報告もあるが、どう考えるべきか?
eGFR<30mL/min/1.73m2であるCKD G4/G5のグループではRAS阻害薬の中止した群と辞めなかった群で5年間経過を見た研究では、透析(-8.3%)は減少したが、心血管イベント(11.9%)や死亡率(13.6%)は上昇した。

参:10254例のRAS系阻害薬が投与されている新規発症eGFR<30ml/min/m2の症例1553例に対してRAS系阻害薬中止による効果を見た。5年間で腎臓代替治療(KRT)は36.1%から27.9%と8.3%低下したが、心血管疾患などによる死亡が40.9%から54.5%に上昇した。
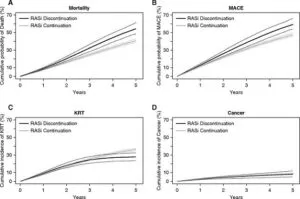
腎臓の悪化は予防できる可能性があるが、心血管疾患などによる死亡が増加する危険があることになる。
JASW 2021 32 424-435
CKD診療ガイドライン2023では第11章 薬物治療の11-4 CQ『CKDステージG4、G5の患者にRA系阻害薬の中止は推奨されるか? に対して
腎代替療法へのリスクに対する影響は不確定であるが、生命予後を悪化させる可能性があるため、CKDステージG4、G5では使用中のRAS系阻害薬を一律に中止しないことを提案する。 としている。
臨床現場胃において、Crが上昇し続けている場面において、心血管疾患の増加を懸念してRAS系阻害薬を投与し続けることは困難である。
ARNIはネプリライシン阻害薬のサクビトリルとRAS阻害薬のバルサルタンの合剤である。
サクビトリルにより降圧ホルモンであるナトリウム利尿ペプチドは増加し、血管拡張、交感神経抑制、利尿・Na利用が認められ、バルサルタンにより昇圧ホルモンであるアンジオテンシン2の働きを抑え、血管収縮を抑制し体液貯留を抑制する。
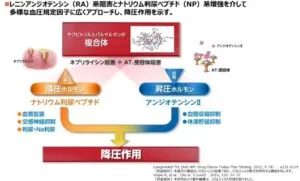
降圧効果もオルメテック20㎎よりも強い。
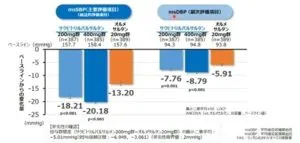
BNPがどのように糸球体に作用しているかというと、
- 輸入細動脈拡張
- 炎症サイトカイン(TNF-α、IL-6)抑制、線維化抑制
- メサンギウム/ポドサイト弛緩作用
であるとされている。
自分が初めて聞いた時には、ARBの作用で糸球体内圧を低下させて腎機能への影響を期待するところ、Sacubitrilの作用で輸入細動脈を拡張してしまうと、糸球体内圧は下がらないのでは、と考えた。
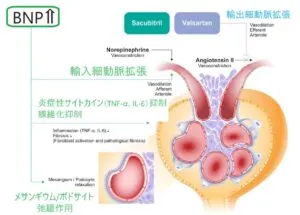
Medical Physiologyで糸球体濾過量を決定する因子を見てみると下図の右下の図に示されているように、糸球体内での濾過は、毛細血管の前半部分でほぼ終わっており、下図の左上図の毛細管の後半部分では、ほとんど行われていないことが示されている。
https://doctorlib.info/physiology/medical/179.html
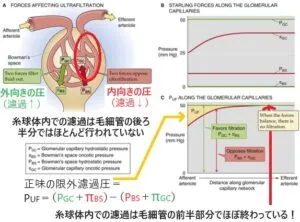
糸球体毛細血管に沿った限外濾過圧(Puf)の変化を考えてみる。
GFRは下の式で表される。
GFR=Kf×Puf
毛細血管濾過定数であるKfは下記の式で表される。
Kf=有効後過面積(S)×糸球体係蹄壁の透過性(k)
この計算式の有効濾過面積が変化する可能性が考えられる。
ARBのみの投与なら輸出細動脈が拡張するのみで、ARNIによる輸入細動脈の弛緩作用のみだったらKfは変わらず、Puf(正味の限外濾過圧)のみ高くなり、GFRは増えるが、糸球体内圧は上昇する可能性がある。ARNIには輸入細動脈拡張作用にメサンギウム/ポドサイト弛緩作用があり、この作用の結果として、有効濾過面積が増えPuf(正味の限外濾過圧)の上昇が緩和され、糸球体内圧を上げずにGFRが増加する可能性が考えられる。
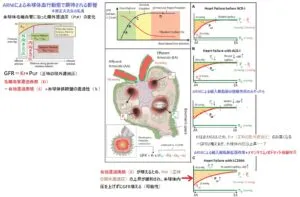
JACC Heart Fail. 2018 Jun;6(6):499-502.
https://www.sciencedirect.com/science/article/pii/S2213177918302178?via%3Dihub
参:
A:安定心不全患者における人定灌流に対する腎適応機構
慢性心不全患者においては心機能障害があり、心拍出量の減少とともに、腎灌流量が減少する。その結果RAAS系の活性化による適応機構をもたらし、アンジオテンシン2による血管収縮を誘発し、糸球体後抵抗の二次的な増加、ひいては、糸球体内圧の上昇を伴う。糸球体後抵抗の増加は、腎灌流が全身血圧の低下に続発して減少しても毛細血管内圧を増価させ、糸球体濾過される腎血流量の割合が増加し、腎灌流が減少しているにもかかわらずGFRの維持を可能にする。

B:腎低灌流へのRAAS阻害薬の影響
大幅に減少した腎血流の状況においてRAAS阻害薬は、腎の自己調節に対抗し、遠心性細動脈のアンジオテンシン2による血管収縮を阻害して糸球体内圧が減少する。その結果濾過率とGFRが低下し、血圧依存性の状況になる。

C:腎低灌流へのARNIの影響
ネプリライシン阻害によりナトリウム利尿ペプチドの働きを増強する。アンギオテンシン2 type1の阻害とネプリライシン阻害が相まって全身血圧及び腎還流圧をさらに低下させ、輸入細動脈の血管弛緩及び輸出細動脈の相対的収縮を引き起こす。その結果、糸球体前抵抗の減少及び糸球体後抵抗の増加は、腎灌流圧の低下にもかかわらず、毛細血管内圧を上昇にさせ、濾過率とGFRを増加させる。毛細血管内圧の上昇と糸球体バリアなどのARNIの直接作用との相互作用により、尿細管でのアルブミンの濾過率が増加し、アルブミン尿の減少に寄与すると考えられる。

Eur Heart J Cardiovasc Pharmacother. 2021 Sep 21;7(5):445-452
https://academic.oup.com/ehjcvp/article/7/5/445/6209744?login=false
犬の実験であるが、アンジオテンシン2を持続投与した条件で、ニトログリセリン追加投与では腎血流や糸球体濾過率は著変ないが、ANPの投与で腎血流や糸球体濾過率はしっかり増加することが示されている。輸入細動脈拡張作用にメサンギウム/ポドサイト弛緩作用による可能性が考えられる。
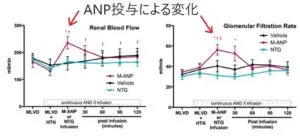
J Am Heart Assoc. 2014 Jan 2;3(1):e000206
https://www.ahajournals.org/doi/10.1161/JAHA.113.000206
まとめると
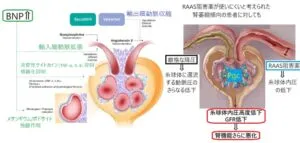
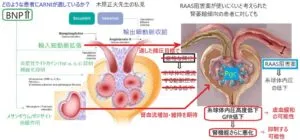
RAAS阻害薬が使いにくいと考えられる腎萎縮傾向の患者に対しては、厳格な降圧ではなく適した降圧目標で治療することにより、輸入細動脈が拡張することにより、糸球体に灌流する動脈圧の低下が緩和され、そこにメサンギウム/ポドサイト弛緩作用により、腎血流増加/維持が期待でき、糸球体内圧の高度の低下・GFR低下を緩和し、腎虚血緩和の可能性が期待でき、腎機能のさらなる悪化を抑制できる可能性が考えられる。
実際の腎保護作用を国際共同第3相試験であるPARAGON-HF試験はHFpEF患者を対象とした試験であるが、複合エンドポイント、心血管死および心不全によるすべての入院は、バルサルタンに比較し、ARNIはHR0.87であったがP=0.06と有意差は出なかった。
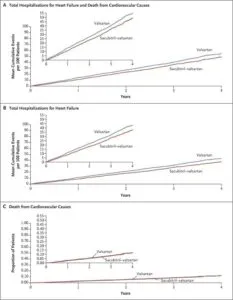
N Engl J Med 2019; 381:1609-1620
https://www.nejm.org/doi/full/10.1056/NEJMoa1908655
しかし、この二次解析では、腎臓の方を見ている。
腎障害の複合アウトカムはARNIのほうがよかった。
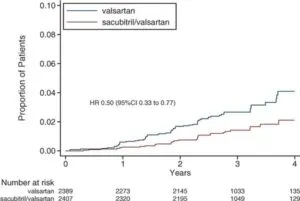
GFRの低下を比較すると0.7の差があって、エビデンスとは言えない結果であるが、腎保護の効果が今後確認される可能性がある。
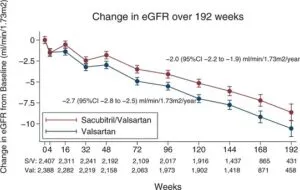
Circulation 2020 142 1236-1245
https://www.ahajournals.org/doi/10.1161/CIRCULATIONAHA.120.047643
まとめると、ARNIが適している患者として、心不全合併CKD、(利尿剤が必要な)体液過剰傾向のCKD、降圧薬多剤使用の難治高血圧患者だけであるが、ARNIを使うことによって、虚血性糸球体の割合が多そうな患者さんでは、RAS阻害薬使用によるGFR低下のリスクを回避できる可能性があり、ARNI使用を考慮してみる価値はある。
腎臓内科の視点から、原疾患、病態に伴う糸球体血行動態異常を十分に考慮し、個別化した降圧目標、降圧薬を選択することも、特にこの高齢化が進んでいる状況では重要である。