川村所長の勉強会参加記録
2023.07.19
高カリウム血症は心不全治療のさい臨床上問題となるか? 大西勝也先生
2023年7月13日
演題「高カリウム血症は臨床上問題となるのか? ~心不全治療における戦略的アジェンダ~」
演者:大西内科ハートクリニック院長 大西勝也先生
場所: Cardio-Renal HK Symposium
内容及び補足「
心不全パンデミック
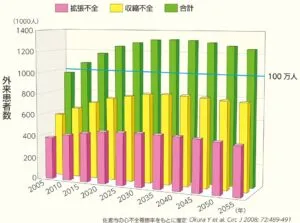
社会の高齢化に伴い、心不全発症数が増加しており、心不全パンデミックの状態にあるといわれている。
2021年時点で推定100万人を超え、2035年まで増加月好き130万人を超えると推計されている。
心不全の標準治療は2021年JCS/JHFSガイドライン フォーカスアップデート版で下図のように、HFpEF、HFmrEF、HFrEFのどこに分類されるかにより判断する図式になっているが、大事なのはどのような順で、ACEi/ARB、βブロッカー、MRA、SGLT2阻害薬を使うかである。
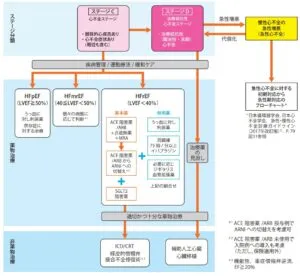
2021年JCS/JHFSガイドライン フォーカスアップデート版 急性・慢性心不全診療
https://www.j-circ.or.jp/cms/wp-content/uploads/2021/03/JCS2021_Tsutsui.pdf
心血管疾患のリスクはCKDで上昇し、尿中アルブミン濃度が上昇するとさらに上昇する。
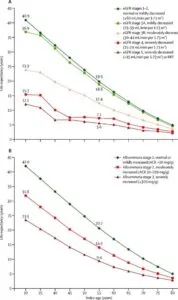
Lancet 382 339-352 2013
https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(13)60595-4/fulltext
加齢に伴い、GFRは低下する。これは、50万ネフロンよりも減少した場合、単一ネフロンの糸球体濾過率の上昇にもかかわらず機能するネフロン数が減少するからである。
健康人の場合にはeGFRは年に0.6~1 mL/min/1.73m2低下する。
高血圧や糖尿病、肥満、アルブミン尿、利尿剤やそのほかのリスクがあると、GFRスロープをより低下させる。心不全患者は心不全がない患者に比べ2.12倍CKDになるリスクが高い。
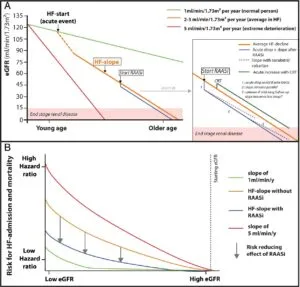
Heart Failure 2020 22 584-603
https://onlinelibrary.wiley.com/doi/10.1002/ejhf.1697
スウェーデンの≦39%の心不全患者の前向きレジストリー研究である。重度の腎不全を伴う心不全患者においてRAS阻害薬を使用することにより全死因死亡率は低下した。

European Heart Journal, Volume 36, Issue 34, 7 September 2015, Pages 2318–2326
https://academic.oup.com/eurheartj/article/36/34/2318/2398249
MRAが心不全に有効であるというエビデンスはたくさんある。PATHWAY-2試験、HOMAGE試験、ALDO-DHF試験、TOPCAT試験、Advanced-HF試験
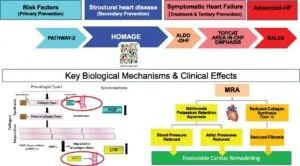
European Heart Journal, Volume 42, Issue 6, 7 February 2021, Pages 684–696,
https://academic.oup.com/eurheartj/article/42/6/684/5993916
60歳以上の収縮期高血圧患者において、2365例の積極治療群(Chlorthalidone 2.5 or 25mg /day、atenolol 25 or 50mg/day、reserpine 0.05 or 0.10mg/day)と2371例のプラセボ群で心不全の入院の頻度を検討したところ心筋梗塞のあるプラセボ群が最も心不全入院が多かった。
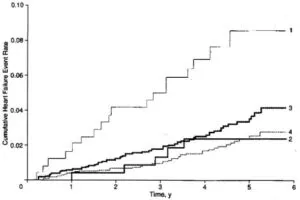
Line 1:MIの既往があるプラセボ群、Line 2:MIの既往がある積極的治療群、Line 3:MIの既往がないプラセボ群、Line 4:MIの既往がない積極的治療群
心不全の発症はAtenololよりもChlorthalidioneのほうが有意に低かった。

JAMA 1997 278 212-216
https://jamanetwork.com/journals/jama/article-abstract/417618
スピロノラクトンよる高K血症の問題点は、スピロノラクトン自体半減期が長く、その上プロドラックであり、代謝産物が薬理学的活性を持ち、さらに長い半減期を有するので、投与患者の38%は、治療中止から3週間まで代謝物が尿中で検出され、投与中止後二週間は降圧効果が半数例で認められる。従って、高カリウム血症が出現した際、自発的な回復は中止直後には期待できないと考えていたほうが良い。
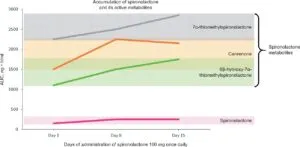
European Heart Journal, Volume 42, Issue 2, 7 January 2021, Pages 152–161,
https://academic.op.com/eurheartj/article/42/2/152/5936792?login=false
Clinical Practice Research Datalink(CPRD)とHospital Episode Statictics(HES)のでーたで18歳以上でCKDステージ3、心不全、難治性高血圧、透析、糖尿病の一つ以上がある患者でRAS阻害薬の投与の有無で高K血症をみた。
931460例のうち310535(33.3%)に高K血症を、187719例(20.2%)に繰り返す高K血症を認めた。
高K血症(≧5.0mmol/L)を認めた症例の33.3%に再度高K血症を認めた。CKD患者では4.45%、心不全患者では42.49%で再度高K血症を認めた。

高K血症の頻度が多くなるとイベントが減る傾向がみられた。
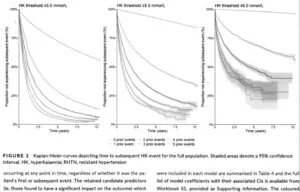
Resistant Hypertension(RHTN)、糖尿病、CKD、心不全(HF)、透析、RAAS系阻害薬使用者においても同様の傾向がみられた。
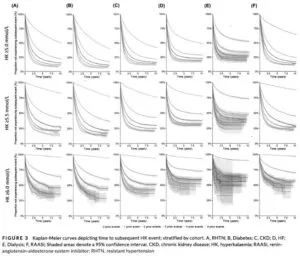
Int J Clin Pract 2021 75 e13941
https://onlinelibrary.wiley.com/doi/abs/10.1111/ijcp.13941
1995年から2012年の間に44799例の30歳以上の高血圧患者を7段階の血清K濃度で死亡率を見てみたところ4.1~4.4 mmol/Lが一番低かった。
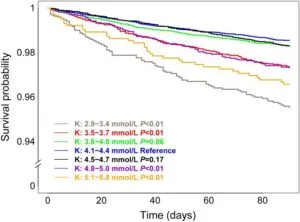
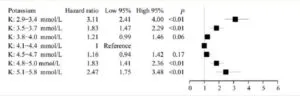
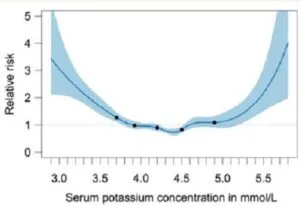
Eur Heart J 38 2017 104-112
https://academic.oup.com/eurheartj/article/38/2/104/2965186
カリウムの有益な効果として以下の表のような効果がある。
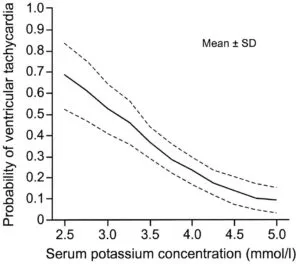
血清K値と心室細動の発生の関係を見ると逆相関の関係がある。
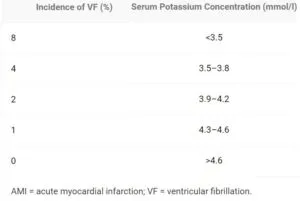
血清Kが4.6mmol/Lを超えると発生しなかった。
利尿薬投与にル左室機能不全患者における不整脈死の相対リスクを見てみると、カリウム保持性利尿薬以外は高値となっている。

血清K値は4.5mmol/L以上に保つのが良いといえる。
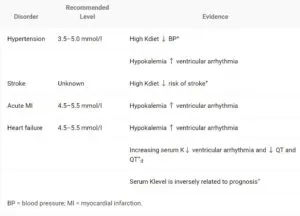
J Am Coll Cardiol. 2004 Jan, 43 (2) 155-161.
https://www.jacc.org/doi/10.1016/j.jacc.2003.06.021
JACCでは心不全標準治療のために血清K値について下記のように分類した。
K<2.5 mEq/L severe hypokalaemia
2.5≦K<3.0 mEq/L moderate hypokalaemia
3.0≦K<3.5 mEq/L mild hypokalaemia
3.5≦K≦5.5 mEq/L normal range
5.5<K≦6.0 mEq/L mild hyperkalaemia
6.0<K≦6.5 mEq/L moderate hyperkalaemia
K>6.5 mEq/L severe hyperkalaemia
JACC Heart Failure 8 961-972 2020
https://www.sciencedirect.com/science/article/pii/S2213177920305680
2000~2012年にかけてきたデンマークで心不全と診断され血清Kが5.0mmol/Lを超えた頻度を見た。
31649例の心不全患者のうち39%に高K血症を認めた。2回目、3回目、4回目の高K血症を経験する頻度は43%、54%、60%であった。心不全があり、CKDのステージが3A、3B、4、5の合併者では26%、35%、44%、48%であった。スピロノラクトンの使用により高K血症のリスクは1.48倍増加し、高K血症がある患者は、ない患者よりも急性期入院が2.75倍、死亡が3.39倍高頻度にみられた。

Journal of the American Heart Association. 2018;7:e008912
https://www.ahajournals.org/doi/full/10.1161/JAHA.118.008912
2003年1月から2018年12月にかけて52253例の患者で48333例経過が終えた。
5.0mmol/Lの高K血症を認めたかどうか、EF40%以下かそうでないか、RAAS系阻害薬が使用されたかどうかで予後を検討した。死亡も3ポイントMACEともに高K血症があるほうが、予後が悪いがそれ以上にRAAS系阻害薬を使わないと予後が悪い可能性が示された。
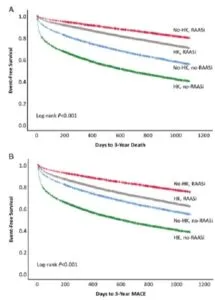
ESC Heart Failure2021;8:691–696
https://onlinelibrary.wiley.com/doi/epdf/10.1002/ehf2.13164
BIOSTAT-CHF試験の結果から高K血症の障害が予後を悪くしたのではなく、高K血症が存在することでRAAS系阻害薬を使用しなかったことが予後を悪くしたと指摘している。

Eur J Heart Fail. 2018 May;20(5):931-932
https://onlinelibrary.wiley.com/doi/10.1002/ejhf.1175
RAAS系およびNatriuretic Peptideの活性化及びACEi/ARBとARNIの作用機序
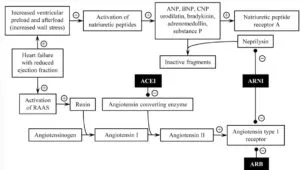
PARADIGM-HF試験結果によりARNIの使用はRAAS系阻害薬を使用するよりもリスクが少ないという結果が示された。K上昇程度も少ない。
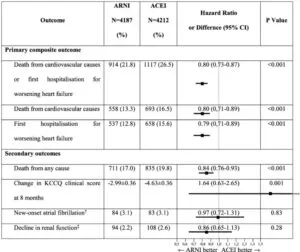
Heart Failure Reviews volume 25, pages393–402 (2020)
https://link.springer.com/article/10.1007/s10741-019-09879-x#Fig1
高K血症による治療薬としてロケルマが上市された。
ロケルマは非ポリマー向き陽イオン交換化合物である。
消化管全体にわたり、カリウムイオンを特異的に捕捉し、水素イオン及びナトリウムイオンと交換する。

臨床試験では、高K血症患者に本罪10gを1日3回2日間反復経口投与したところ、
血清K値は投与開始後1時間から低下し正常値に達するのに24~48時間程度を要した。その後ロケルマは補足したカリウムとともに糞便中に排泄される。
https://med.astrazeneca.co.jp/player/movie_page.html?cmpid=lok_moa01
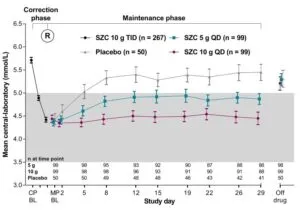
ESC Heart Failure 2020; 7: 55–65
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7083449/pdf/EHF2-7-54.pdf
ロケルマの副作用としては
低K血症(3.5mmol/L以下:11.5%)、うっ血性心不全(0.5%)が重篤な副作用として着刺されているが、それ以外の副作用としては、浮腫、便秘があげられているが、大きな問題になることは少ない。
file:///C:/Users/jeffbeck/Downloads/LOK05_PI.pdf
私が高K血症患者に対して診療上考えている基本的な閑雅を下記に記す。
K値が高値でも安定しているか、緩徐に上昇している場合には、6.0 mEq/L以上から、K値が急に上昇してきた場合や腎機能も急に悪化している場合には、5.5 mEq/L以上から再検査を行う。
MRAの投与がなされている患者の場合には、
頑張ってMRAを入れた腎機能が悪い患者の場合には、MRAはそのまま投与を続け、K値の上昇が生じた場合には最初からK吸着剤を投与する。
普通にMRAを投与開始した患者においては、MRAを半量にして一週間後にK値を再検査する。
eGFR≧45、Cr<2.0の症例ではMRAは継続し、eGFR<45、Cr≧2.0の場合には減量や中止を考慮する。
またeGFRが30前後の症例においては一週間処方、45前後の症例では2週間処方にして、値の水死を見ている。
最後に、高K血症患者を診た際に必ず考慮すべきことは、本当に高K決勝になっているかということである。
血清K値に影響をおよぼす因子としては以下のものがある。
- 採血後検査までの時間 8時間常温で血球・血小板破壊 20度5上昇
- 採血後検体保存時の温度
- 駆血帯の影響(グーパーの繰り返し)アシドーシスでpHが1低下するとK値は0.7mEq/L上昇
- 溶血・血小板の破壊 血小板の破壊がわかりにくい
参:血清Kについての一般的な知識
カリウムの排泄経路尿から90%便10%、細胞内98%細胞外2%
細胞内にKを取り込むにはインスリンが必要
β2刺激でATPaseを活性化してK濃度は低下する。
アシドーシスでpH 0.1下がるとカリウムは0.4 mEq/L下がる。
高血糖で血漿浸透圧が上がると細胞内からK流出してK上昇する
有酸素運動 0.4mEq/L、中等度運動 1 mEq/L、強度運動 2 mEq/L上昇
運動時にカテコラミンが放出されて細胞に取り込まれる。
低カリウム血症の原因
- 摂取不足
- 細胞内への過度の移動
- 腎からの過剰排泄:サイアザイド(0.6mEq/L低下)、ループ利尿薬(0.3mEq/L低下)
- 腸管からの過剰排泄:下痢など
高カリウム血症の原因
- 過剰摂取
- 細胞内への移動の抑制
腎からの排泄障害:eGFR<40にならないとKは上昇しない