川村所長の勉強会参加記録
2014.11.25
グルカゴンからみた2型DMの薬物療法の考え方 北村教授
2014年11月12日 崎陽軒本店
演題「グルカゴンからみた2型糖尿病の薬物療法の考え方」
演者:群馬大学生体調節研究所教授 北村忠弘先生
内容及び補足「
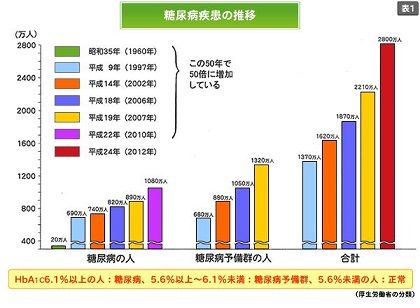
糖尿病及びその疑い患者は1980年代には日本人の100人に一人ぐらいの割合であったが、2010年には6人に一人となっている。1960年からの50年間で50倍にもなっている。これだけ急増した疾患は人類史上他にはない。
糖尿病の原因としては肝臓、筋肉、脂肪組織におけるインスリン抵抗性と、唯一のインスリン低下作用を持つインスリンを分泌するβ細胞障害、血糖上昇作用を有するグルカゴンを分泌するα細胞障害がある。
2003年に行われたヒトゲノムワイド解析の結果わかったことは、糖尿病感受性遺伝子と考えられるものが100個以上存在するが、その8割以上が膵ラ氏島関連遺伝子であり、今まで積極的に研究されたり、対応策が打ち出されてきたインスリン抵抗性に関するものが2割にも満たないことは少し意外であった。
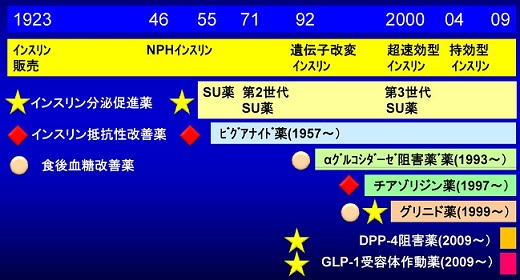
研修医になりたての頃の糖尿病治療薬はSU薬とビグアナイドのみであり、乳酸アシドーシスの副作用のためビグアナイドはほとんど使用されておらず、SU薬療法とインスリン治療が主流であった。
1995年ごろからαGIやチアゾリジン誘導体などが発売され、2010年には、ビグアナイド系が見直され、メトグルコが発売され、翌年インスリン分泌促進薬であるシュアポストも発売された。その後GLP-1受容体作動薬や、DPP-Ⅳ阻害薬、SGLT2(sodium-dependent glucose transporter2)が発売され、治療薬に幅が出てきた。
Roger H. UngerとAlan D. Cherringtonが2012年に以下のように述べている。
1921年インスリンが発見され、インスリン投与によりIDDM患者の血糖値が速やかに改善し、患者予後が改善されることより、糖尿病の病態は、インスリンが中心であるというinsulinocentric説が翌年に唱えられた。
1923年にグルカゴンが発見されたが、測定系もないことからほとんど注目されてこなかった。
1959年にRIA法による測定系が開発されたが、精度に問題があるため、グルカゴンの研究はほとんど進展をみなかった。
1975年にRoger H. Ungerらが、糖尿病の病態は、インスリンだけでなく、グルカゴンも影響しているというBi-hormonal説を提唱したが、ほとんど注目されなかった。
しかし、2011年に、Roger H. Ungerは糖尿病の病態の中心的な役割をなしているのは、グルカゴンであるというGlucagonocentric説を唱え、グルカゴンが注目を浴びるようになってきた。日本糖尿病学会においても、2013年に初めて、グルカゴンルネッサンスというタイトルでシンポジウムを開催し、本年度も同様のタイトルでシンポジウムを開催し、多数の方に参加してもらえた。
http://www.jci.org/articles/view/60016
Roger H. UngerがGlucagonocentric説を唱える根拠となった実験を見ていこう。
① Aidan S. Honcockらは、通常マウス(control)とα-cell transcription factor欠損マウス(Arx)の二群に 糖尿病マウスを作製する際によく用いられる薬剤streptozotocin(STZ)を投与して、血糖値の変化を見た。Control群は徐々に血糖値が上昇してくるが、Arx群では血糖値の上昇がみられなかった。このことは、グルカゴンが存在しないときには、インスリンの欠乏のみで血糖値の上昇が来ないことを示唆しているといえる。
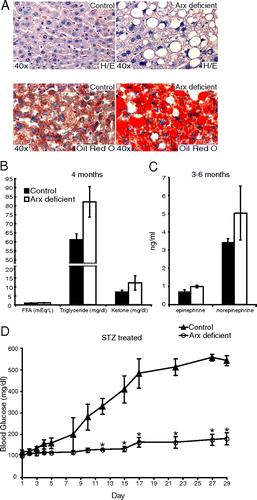
http://press.endocrine.org/doi/full/10.1210/me.2010-0120
② Lee Yらはα細胞欠損マウスではなく、グルカゴン受容体欠損マウス(Gcgr-)を作製して同様の実験を試みている。
下図のCのように、グルカゴン受容体欠損マウスGcgr-では、STZを投与してインスリンの分泌がなくなっても、血糖値が上昇してこなかった。このことは、グルカゴンが存在していても、肝臓にグルカゴン受容体が存在しない=肝臓にグルカゴンが作用しないと、血糖値が上昇してこないことを示している。
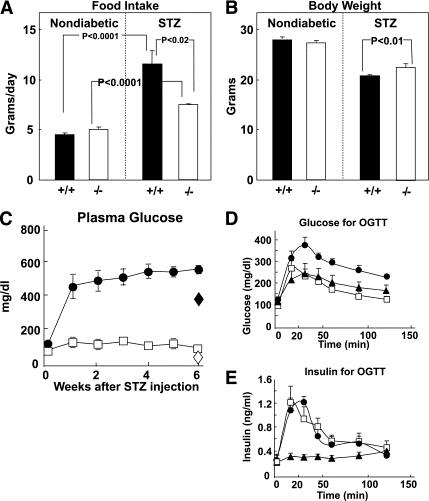
A: Comparison of food intake in nondiabetic and STZ-treated Gcgr+/+ (■) and Gcgr−/− (□) mice (n = 6). B: Comparison of body weight in Gcgr+/+ (■) and Gcgr−/− (□) before and after STZ induction of β-cell destruction. C: Comparisons of weekly nonfasting glucose levels in Gcgr+/+ (●) and Gcgr−/− (□) after STZ-induced β-cell destruction, and overnight fasting glucose levels for Gcgr+/+ (♦) and Gcgr−/− (◇) at the end of the study (n = 6). D: Glucose values for oral glucose tolerance test (OGTT) (2 g/kg) performed after a 16-h fast in normal Gcgr+/+ (●), Gcgr−/− (☐), and STZ-treated Gcgr−/− (▲) mice (n = 4). E: Insulin levels for OGTT in normal Gcgr+/+ (●), Gcgr−/− (☐), and STZ-treated Gcgr−/− (▲) mice (n = 4).
http://www.ncbi.nlm.nih.gov/pubmed/21270251
③ さらにLee Yらはアデノウイルスルを用いて、このグルカゴン受容体欠損マウスGcgr-にグルカゴン受容体の遺伝子を導入して、血糖値の推移をみている。下図DのようにAdv-GcrR感染群は血糖値の上昇が、アデノウイルス感染の効果が持続している8日目までは高血糖が持続し、遺伝子発現が消失する8日目以降においては、速やかにグルカゴン受容体欠損マウスと同じ血糖値にまで低下している。
このことは、グルカゴンが肝臓に作用している期間においてのみ、血糖値の上昇がみられ、糖尿病の病態が発現していることを示唆している。
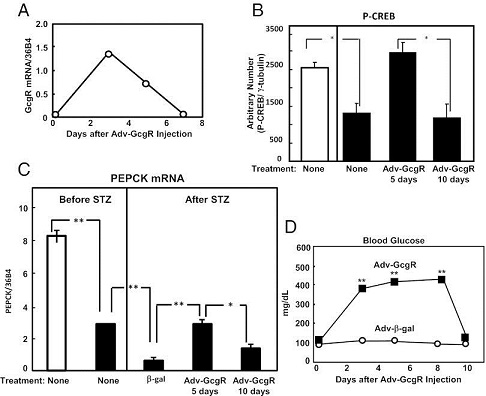
The effects of transient transgenic expression of GcgR in the liver of insulin-deficient GcgR-null mice upon markers of glucagon action and upon blood glucose levels. (A) Pattern of liver GcgR mRNA expression before and after injecting Adv-GcgR into insulin-deficient GcgR−/− mice. (B) Densitometric measurements of CREB, a transducer of glucagon action, in GcgR−/− mice before, during, and after expression of adenovirally delivered GcgR cDNA (P < 0.01). (See Fig. S1 for a representative immunoblot). (C) PEPCK mRNA in intact WT (open column) and in streptozotocinized GcgR−/− mice (solid column) before and at 5 and 10 d after the administration of adenovirus containing the GcgR cDNA (*P < 0.01; **P < 0.001). (D) Blood glucose levels (mean ± SEM) in GcgR−/− mice injected adv-β-gal (○) and Adv-GcgR (■) after destruction of β-cells by high-dose STZ (**P < 0.001).
http://www.ncbi.nlm.nih.gov/pubmed/22891336
これらの実験から見えてくることは、インスリン分泌や作用がなくなっても、それだけでは血糖値の上昇はなく、インスリンの分泌や作用がなくなったことに加えて、グルカゴンの作用が存在して、はじめて血糖値が上昇するということである。
メトホルミンなどのビグアナイド系薬剤は、50年ほど前から肝の糖産生を抑制する血糖降下薬として使われてきたがその作用機序の詳細は不明であった。
10年ほど前に、メトホルミンの血糖降下作用は、ATP活性化プロテインキナーゼ(AMPK)を活性化して肝臓の糖放出の抑制と筋肉のグルコース取り込みの更新による機序が示された。
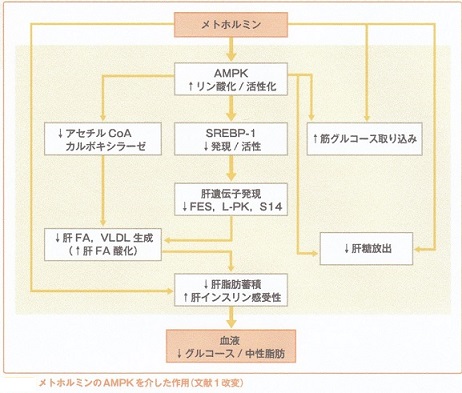
しかし、2010年にAMPKやその上流のLKB1の欠損した肝臓や肝細胞でもメトホルミンの血糖降下作用が認められるので、それ以外の作用が存在することが想定されていた。
http://www.ncbi.nlm.nih.gov/pubmed/20577053
肝細胞において、グルカゴンは、グルカゴン受容体を刺激してATPをcAMPに変換し、このcAMPがPKA介して、肝臓における糖新生を促進している。
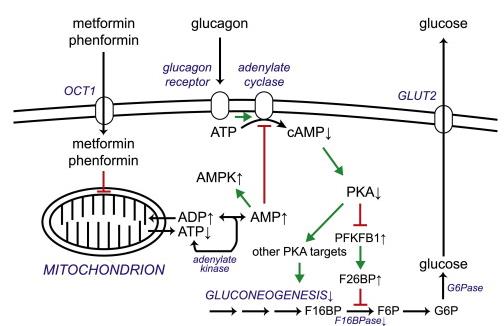
http://www.ncbi.nlm.nih.gov/pubmed/23292513
2013年にRussell A. Millerらにより、メトホルミンが容量依存的に、この糖新生を抑制することにより、血糖値を低下させているということが示された。
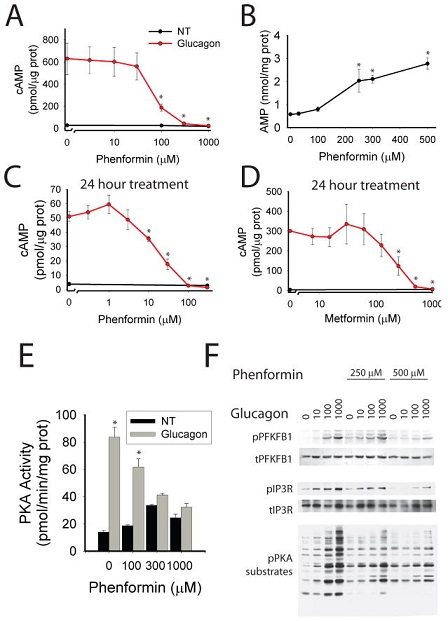
Biguanides inhibit cAMP production
A. Primary hepatocytes were incubated with the indicated phenformin concentrations for 2 hours, 5 nM glucagon for 15 minutes, lysed, and assayed for total cellular cAMP and protein. N=4 for each point. B. Primary hepatocytes incubated with the indicated concentration of phenformin for 2 hours were extracted with perchloric acid and cellular nucleotides quantified by HPLC. N=4 for each point. C-D. Primary hepatocytes were incubated with the indicated concentration of phenformin (C) or metformin (D) for 24 hours, treated with 5 nM glucagon, lysed, and assayed for total cellular cAMP. N=4 for each point. E. Primary hepatocytes were incubated with the indicated concentrations of phenformin for 2 hours, treated with 5 nM glucagon, lysed, and PKA kinase activity determined. N=6 for 0 and 1000 μM phenformin groups, N=4 for 100 and 300 μM phenformin groups. F. Primary hepatocytes were incubated with phenformin for 2 hours, then glucagon, and protein was analyzed by western blot with the phospho-PKA substrate motif antibody, total and phospho-PFKFB1 antibodies, and total and phospho IP3R antibodies. Error bars represent standard error.
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3573218/figure/F1/
メトホルミンの低用量は肝細胞や骨格筋での糖の取り込みを促進し、高容量では肝細胞でのグルカゴンによる糖新生をブロックして、より血糖値を低下させていることが示唆された。
グルカゴンの詳細な研究が近年まで、積極的に行われてこなかった理由には、下記のようなものが考えられている。
① グルカゴン分泌細胞数が少ないこと(膵ラ氏島の細胞のうちβ細胞が約80%、α細胞が約10%)
② グルカゴンの分解が早く不安定
③ グルカゴン分泌細胞であるα細胞の良い培養細胞株がないこと
④ グルカゴン測定系が信頼できない
グルカゴンはプログルカゴンからプロセッシングを受けて小さくなるが、様々な切れた田があり、それによりいろいろな物質が産出され、複数のものを、グルカゴンとして測定していたため、正確な測定が困難であった。
アミノ酸配列をもとにプログルカゴンから作られるものを並べてみると下のようになる。
以前は、グルカゴンの抗体はGlicentinやOxytomodulinなどの複数のものを同時に測定していた。その後に開発されたいくつかのキットでも、グルカゴンのC末端に対する抗体で測定すると、グルカゴンの他にGlicentin1-61も測定されるし、N末端に対する抗体測定ではOxytomodulinも測定されてしまう。
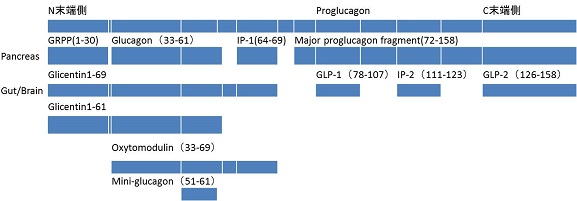
GLP:glucagon-like peptide、IP:insulinotropic polypeptide
http://books.google.co.jp/books?id=1W2M1lnHeccC&pg=PA191&lpg=PA191&dq=proglucagon+%E3%81%A8Glicentin1-69&source=bl&ots=wDHAf56k-z&sig=79tz7zM4QrHMEe0oP6hGqmilw5I&hl=ja&sa=X&ei=VMFyVOWLGce2mwWc-oKACA&ved=0CB8Q6AEwAA#v=onepage&q=proglucagon%20%E3%81%A8Glicentin1-69&f=false
現在、Glucagonの両末端をサンドイッチで測定するキットを開発中である。
現在開発されている糖尿病の治療薬は、たくさんあり、近年開発されている糖尿病治療薬は多数に上る。
① グルコキナーゼ活性化薬:肝臓での糖の取り込みおよび膵臓からのインスリン分泌を促進して血糖を低下する薬剤。
② GPR119受容体アゴニスト:消化管と膵臓に存在する受容体であるG蛋白質共役型受容体119は、生物活性脂質と相互作用して、グルコース依存性インクレチンおよびインスリンの分泌を促進する。膵臓のβ細胞からのインスリン分泌を促進し、小腸からのインクレチンGLP-1の分泌を促して血糖値を低下する薬剤。
など
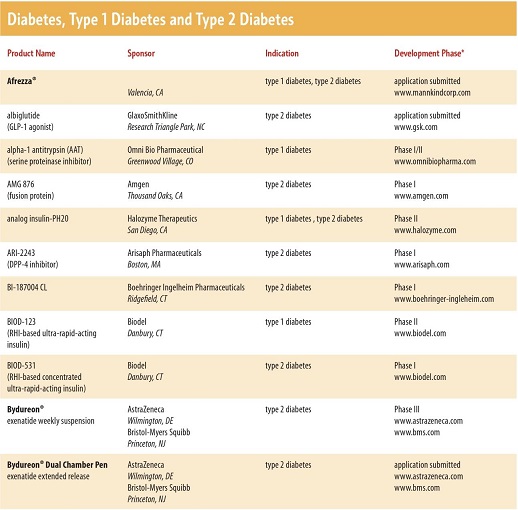
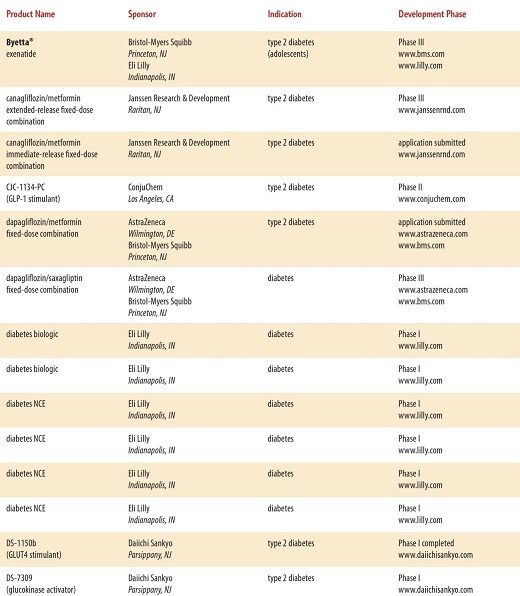
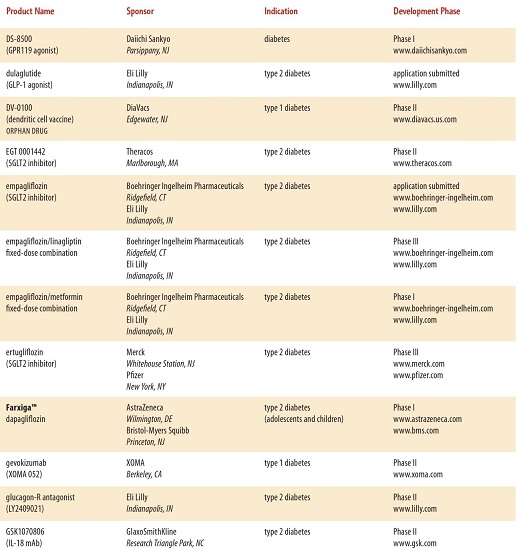
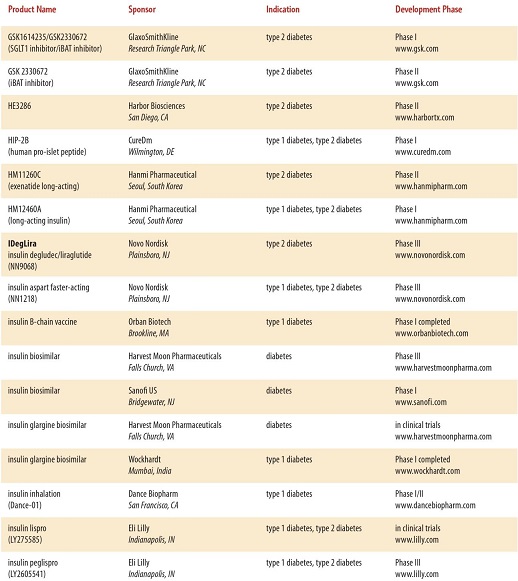
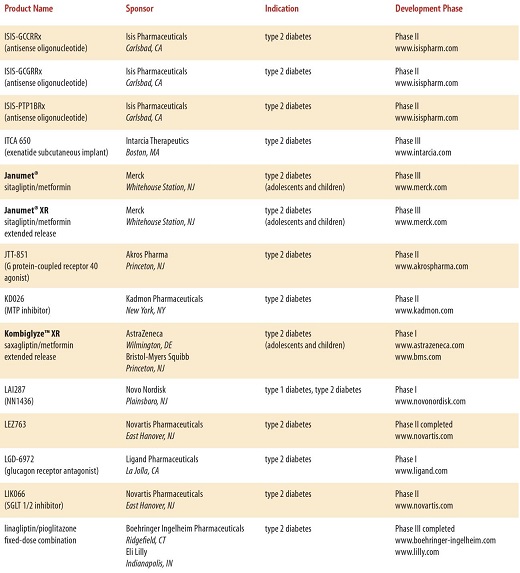
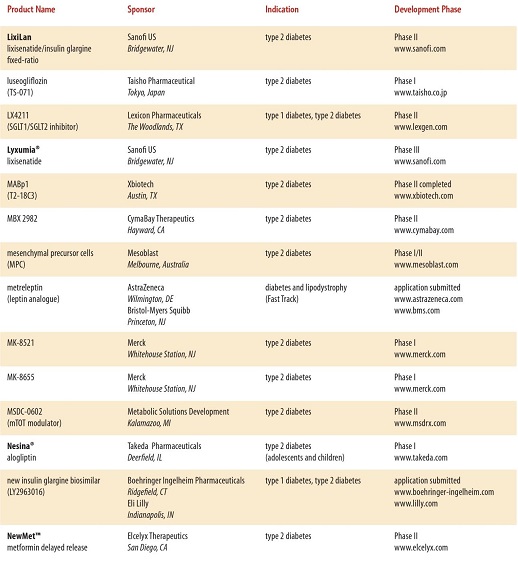
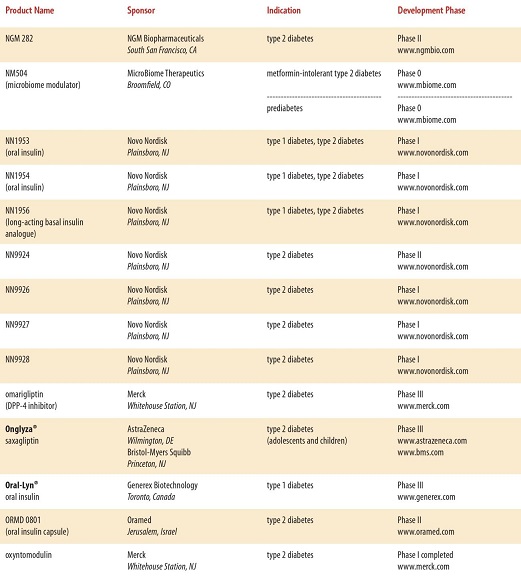
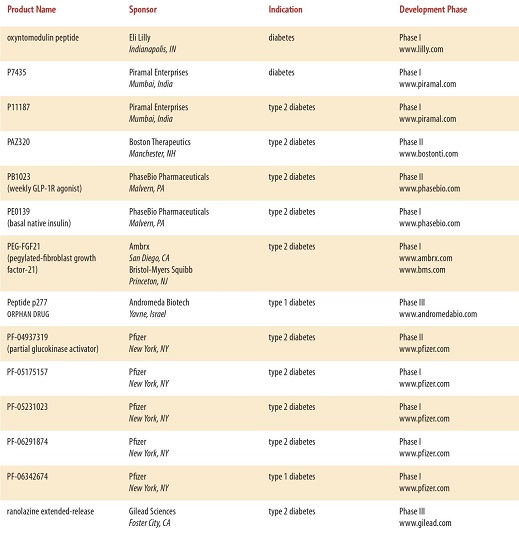
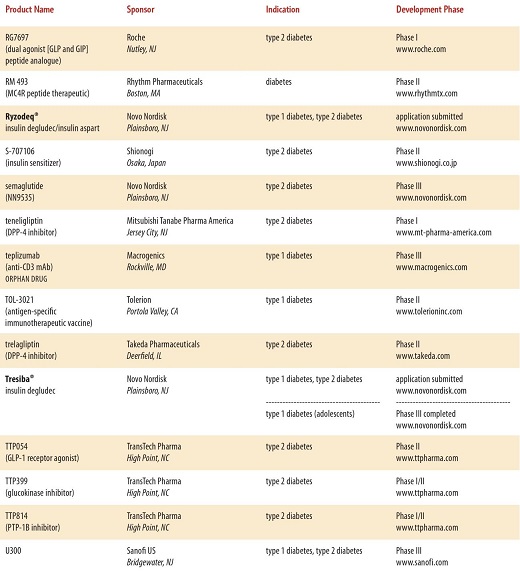
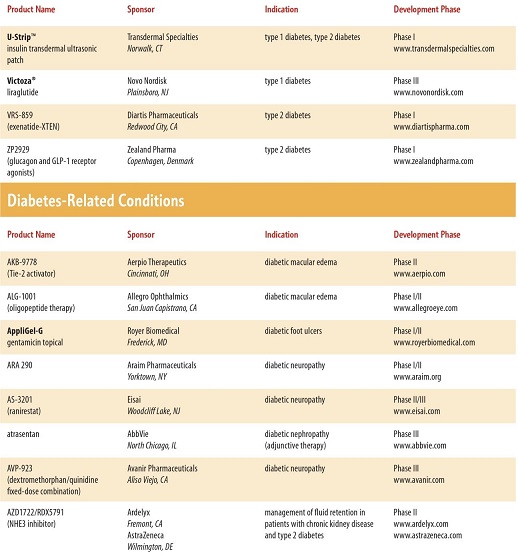
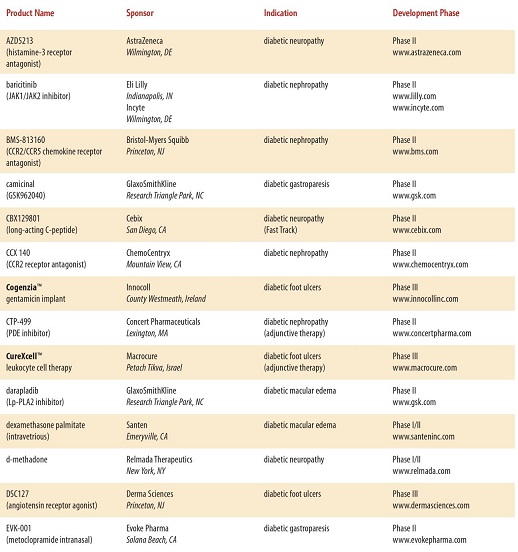
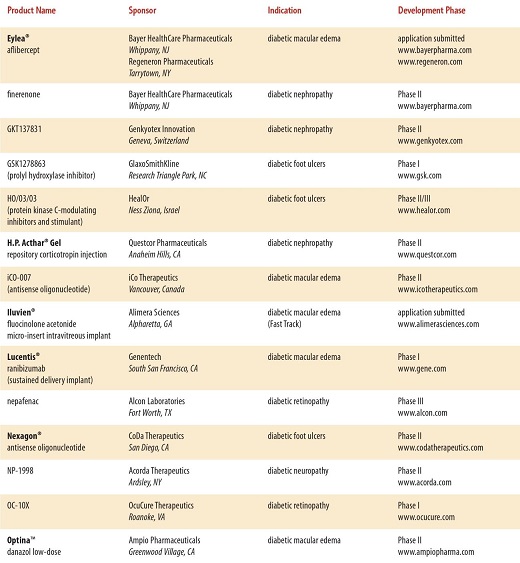
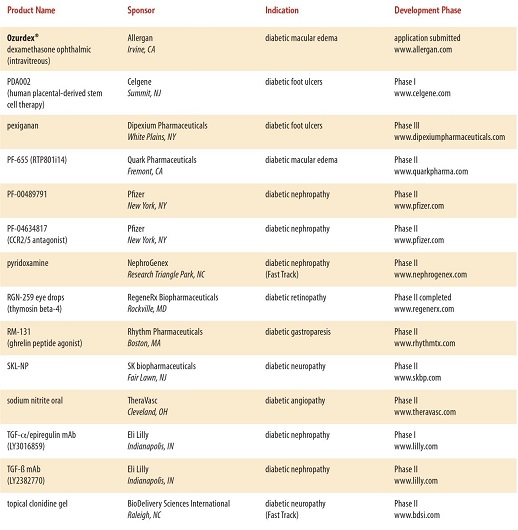
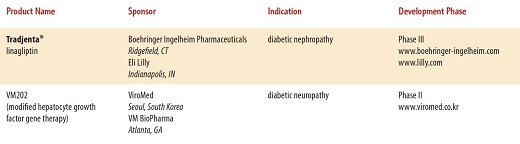
と、多数にのぼり、糖尿病専門医でも対応困難となる可能性もある。種々のデーターを入力し、最適な治療薬をコンピュータで判断するような時代になるかもしれない。
http://www.phrma.org/sites/default/files/pdf/diabetes2014.pdf